تمایز سلولی
تمایز سلولی یا دگرگونی یاختهای فرآیندی است که طی آن سلولها از نظر ویژگیهای عملکردی به سطح بالاتری گذار میکنند. عملیات «تمایز» در طول رشد و گسترش یک جاندار پرسلولی (از تکسلولی تخم بارور∗ به سامانهای پیچیده از سلولها و بافتهای گوناگون) بارها صورت میگیرد.
در زیستشناسی تکوینی، تمایز سلولی فرآیندی است که یک سلول از یک نوع به نوعی دیگر تغییر میکند.[1][2] اغلب یک سلول به یک نوع تخصص یافته تر تغییر میکند. فرایند تمایز چندین بار در طول تکوین یک ارگانیسم چند سلولی که از یک زیگوت (سلول تخم) ساده به یک سیستم پیچیده از انواع بافتها و سلولها تغییر میکند، رخ میدهد. تمایز در طول دوران بزرگسالی همچنان ادامه پیدا میکند. برخی از تمایزها در پاسخ به مواجهه با آنتیژن رخ میدهند. تمایز به طرز چشمگیری باعث تغییر اندازه، شکل، پتانسیل غشاء، فعالیت متابولیکی و پاسخ دهی به سیگنالها در سلول میشود. این تغییرات عمدتاً ناشی از اصلاحات بسیار کنترل شده در بیان ژن و موضوع مطالعه در اپی ژنتیک (epigenetics) هستند. با چند استثناء، تمایز سلولی خود به تنهایی تقریباً هرگز باعث تغییر در توالی DNA نمیگردد؛ بنابراین، سلولهای مختلف میتوانند ویژگیهای فیزیکی بسیار متفاوتی داشته باشند با وجودی که ژنوم یکسانی دارند.
سطوح مختلفی از توانایی سلول برای تمایز به انواع دیگر سلول، وجود دارد. سلولی که میتواند به همهٔ انواع سلولها، از جمله بافت جفتی تمایز یابد، با عنوان همه توان (totipotent) شناخته میشود. در پستانداران، تنها سلول زیگوت و بلاستومرهای بعد از آن همه توان هستند، در حالی که در گیاهان بسیاری از سلولهای تمایز یافته میتوانند با تکنیکهای سادهٔ آزمایشگاهی همه توان شوند. سلولی که میتواند به همهٔ انواع سلول از یک ارگانیسم بالغ تمایز یابد، پرتوان (pluripotent) نامیده میشود. چنین سلولهایی در گیاهان رده بالاتر سلولهای مریستماتیک (meristematic) و در حیوانات سلولهای بنیادی جنینی (embryonic stem cells) نامیده میشوند، هر چند برخی گروهها حضور سلولهای همه توان بزرگسال را گزارش میدهند.
القای بیان چهار عامل رونویسی Oct4، Sox2، c-Myc و Kfl4 (عوامل Yamanaka) از طریق ویروس برای ایجاد سلولهای پرتوان (iPS) از فیبروبلاستهای بالغ کافی است.[3]
یک سلول چندتوان (multipotent)، سلولی است که میتواند به چندین سلول مختلف اما مرتبط به هم تمایز یابد. سلولهای کم توان (Oligopotent)، بسیار محدود تر از سلولهای چندتوان هستند، اما هنوز هم میتوانند به تعداد کمی از انواع سلولهای مرتبط به هم تمایز یابند. در نهایت، سلولهای تک نوان (unipotent) هستند که تنها میتوانند به یک نوع سلول تمایز یابند، اما توانایی خودنوزایی (self-renewal) دارند.[4] در سیتوپاتولوژی (cytopathology)، سطح تمایز سلولی به عنوان یک شاخص اندازهگیری پیشرفت سرطان مورد استفاده قرار میگیرد. درجه (Grade) نشانگر میزان تمایز یک سلول در یک تومور است.[5]
انواع سلولهای پستانداران
سه دستهٔ اصلی از سلولها، بدن پستانداران را تشکیل میدهند:
سلولهای زایا (germ cells)،
سلولهای پیکری (somatic cells)
و سلولهای بنیادی (stem cells).
هر یک از حدود ۱۰۰ تریلیون (۱۰۱۴) سلول در یک انسان بالغ دارای رونوشت (کپی) یا رونوشتهای خود از ژنوم است به جز انواع خاصی از سلولها، مانند سلولهای (گلبولهای) قرمز خون، که فاقد هسته در حالت کاملاْ تمایز خود هستند. اکثر سلولها دیپلوئید (diploid) هستند که دو رونوشت از هر کروموزوم دارند. چنین سلولهایی، سلولهای سوماتیک، بیشتر بدن انسان را تشکیل میدهند، مانند سلولهای پوستی و عضلانی. سلولها تمایز مییابند تا برای عملکردهای متفاوت، تخصص یابند.[6]
سلولهای ردهٔ زایا، هر رده ای از سلولها هستند که به گامتها -تخمکها و اسپرم تمایز مییابند و بدین سان در طی نسلها باقی میمانند. از طرف دیگر، سلولهای بنیادی توانایی دارند تا برای دورههای نامحدود تقسیم شوند و به سلولهای تخصص یافته تمایز پیدا کنند.
تکوین زمانی آغاز میشود که یک اسپرم، تخمک را بارور میکند و یک سلول واحد را ایجاد میکند که توانایی تشکیل یک ارگانیسم کامل را دارد. در اولین ساعات پس از لقاح، این سلول به سلولهای کاملاً مشابه تقسیم میشود. در انسانها، تقریباً چهار روز پس از لقاح و بعد از چندین چرخهٔ تقسیم سلولی، این سلولها شروع به تخصصی شدن میکنند، و یک کُرهٔ توخالی از سلولها به نام بلاستوسیست (blastocyst) را شکل میدهند.[7] بلاستوسیست یک لایهٔ بیرونی از سلولها را دارد، و درون این کرهٔ توخالی، دسته ای از سلولها به نام تودهٔ سلولی داخلی (inner cell mass) قرار دارد.
سلولهای تودهٔ سلولی داخلی عملاً همهٔ بافتهای بدن انسان را شکل دهند. اگرچه سلولهای تودهٔ سلولی داخلی میتوانند عملاً هر نوع سلولی را که در بدن انسان یافت میشود، تشکیل دهند، آنها نمیتوانند یک ارگانیسم را ایجاد کنند. این سلولها به عنوان پرتوان شناخته میشوند.[8]
سلولهای بنیادی پرتوان متحمل تخصص یافتگی بیشتری میشوند و به سلولهای پیش ساز چندتوان (multipotent progenitor cells) تبدیل میشوند که سپس این سلولها به سلولهای عملکردی تبدیل میگردند. نمونههایی از سلولهای بنیادی و پیش ساز عبارتند از
- سلولهای گلیال شعاعی (radial glial cells) (سلولهای بنیادی عصبی جنینی) که به نورونهای تحریکی در مغز جنین در طی فرایند نوروژنزیز تبدیل میشوند.[9][10][11]
- سلولهای بنیادی خون ساز (hematopoietic stem cells) (سلولهای بنیادی بزرگسال) از مغز استخوان که باعث ایجاد گلبولهای قرمز، گلبولهای سفید و پلاکتها میشوند.
- سلولهای بنیادی مزانشیمی (mesenchymal stem cells) (سلولهای بنیادی بزرگسال) از مغز استخوان که باعث ایجاد سلولهای استروما (stromal cells)، سلولهای چربی و انواعی از سلولهای استخوانی میشوند.
- سلولهای بنیادی اپیتلیال (epithelial stem cells) (سلولهای پیش ساز) که انواع مختلفی از سلولهای پوستی را تولید میکنند.
- سلولهای عضلانی ماهواره ای (muscle satellite cells) (سلولهای پیش ساز) که در تمایز بافت عضلانی مشارکت میکنند.
مسیری که توسط مولکولهای چسبنده سلولی ای که شامل چهار آمینو اسید آرژنین، گلایسین، آسپارژین و سرین هستند، هدایت میشود به عنوان بلاستومر سلولی ایجاد میشود. این بلاستومر از یک بلاستولای تک لایه ای به سه لایهٔ اولیه سلولهای زایا (germ cells) در پستانداران به نامهای اکتودرم (ectoderm)، مزودرم (mesoderm) و اندودرم (endoderm) (به ترتیب از نزدیکترین (بیرونی) به دورترین (درونی) لایه) تمایز مییابد. در نهایت اکتودرم منجر به تشکیل پوست و سیستم عصبی میشود، مزودرم استخوانها و بافت ماهیچه ای را تشکیل میدهد و اندودرم بافتهای ارگانهای داخلی را شکل میدهد.
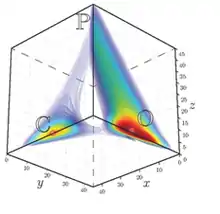
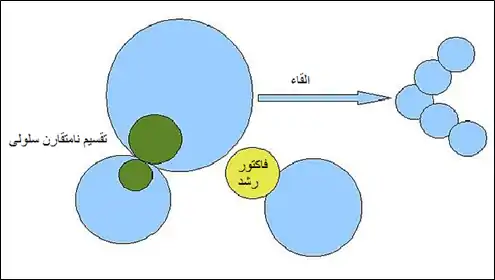
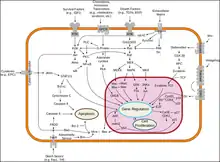
تمایز سلولی در مگس سرکه
در مگس سرکه، مورفوژنها به دو دسته تقسیم میشوند:
- ژنهای کارکرد تخم بارور (به انگلیسی:Zygotic acting)
- ژنهای اثر مادری (به انگلیسی:Maternal effect)
چهرسازهای دستهٔ دوم توسط ۱۵ سلول پرستار که اطراف تخمک در هنگام تخمکسازی (به انگلیسی:Oogenesis) قرار دارند با شیب خاصی در تخمک قرار میگیرند. این سلولهای پرستار توسط دریچههای حلقوی با تخمک ارتباط دارند. در اطراف این مجموعه ۱۶ سلولی حدود ۱۰۰۰ سلول فولیکولی قرار دارد. یکی از اعمال این سلولهای فولیکولی ایجاد پوستهٔ تخم است.
سلول تخم ابتدا رویانلایه (به انگلیسی:Blastoderm)را تشکیل میدهد و بعد با ایجاد فرورفتگی به رودهسا (به انگلیسی:Gastrula) تبدیل میشود. در رودهسا دو فرورفتگی به نامهای شیار سر (به انگلیسی:cephalic furrow) و شیار شکمی (به انگلیسی:ventral furrow) وجود دارند.
تمایز سلولهای بنیادی
روشهای مرسوم در تمایز سلولهای بنیادی در محیط برون تن شامل استفاده از تعدادی مولکولهای مختلف واسطه به عنوان مثال مولکولهای کوچک یا فاکتورهای رشد میباشد.[12]
به عنوان مثال پوشش نانو فایبرها با فسفات کلسیم باعث تمایز سلولهای مزانشیمال انسانی به سمت استخوان خواهد شد. از طرف دیگر مشخص شدهاست که سلولهای بنیادی به سیگنالهای فیزیکی محیط اطراف نیز حساس هستند. سلولهای مزانشیمال میتوانند بر اساس هندسه سطح در مسیر تمایز به دو دودمان سلولی شامل سلولهای چربی یا استخوان قرار گیرند. تغییر در هندسه سطح در تنظیم اسکلت سلولی و چسبندگی موضعی سلول با اعمال محدودیت بر روی پهن شدگی سلولی و در نهایت تأثیر بر روی مسیرهای سیگنال سلولی باعث تمایز سلولهای بنیادی میشود. به عنوان مثال بسترهای نانو فایبری که به صورت موازی ریسیده شده در مقایسه با بسترهای نانو فابری که به صورت درهم ریسیده شدهاست تمایز سلولهای C17.2 تأثیر بیشتری داشتهاست. تحقیقات دیگری نشان دادهاست که سختی سطح، تحریکهای الکتریکی و … نیز بر تمایز سلولهای بنیادی تأثیر خواهد داشت.[13][14][15]
منابع
- 2. Slack, J.M.W. (2013) Essential Developmental Biology. Wiley-Blackwell, Oxford.
- 3. Slack, J.M.W. (2007). "Metaplasia and transdifferentiation: from pure biology to the clinic". Nature Reviews Molecular Cell Biology. 8 (5): 369–378. PMID 17377526. doi:10.1038/nrm2146.
- 4. Takahashi, K; Yamanaka, S (2006). "Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors". Cell. 126 (4): 663–76. PMID 16904174. doi:10.1016/j.cell.2006.07.024.
- 5. Schöler, Hans R. (2007). "The Potential of Stem Cells: An Inventory". In Nikolaus Knoepffler; Dagmar Schipanski; Stefan Lorenz Sorgner. Humanbiotechnology as Social Challenge. Ashgate Publishing. p. 28. ISBN 978-0-7546-5755-2.
- 6. "NCI Dictionary of Cancer Terms". National Cancer Institute. Retrieved 1 November 2013.
- 7. Lodish, Harvey (2000). Molecular Cell Biology (4th ed.). New York: W. H. Freeman. Section 14.2. ISBN 0-7167-3136-3.
- 8. Kumar, Rani (2008). Textbook of Human Embryology. I.K. International Publishing House. p. 22. ISBN 9788190675710.
- 9. D. Binder, Marc; Hirokawa, Nobutaka; Windhorst, Uwe (2009). Encyclopedia of Neuroscience. Springer. ISBN 3-540-23735-6.
- 10. Rakic, P (October 2009). "Evolution of the neocortex: a perspective from developmental biology". Nature Reviews. Neuroscience. 10 (10): 724–35. PMC 2913577. PMID 19763105. doi:10.1038/nrn2719.
- 11. Lui, JH; Hansen, DV; Kriegstein, AR (8 July 2011). "Development and evolution of the human neocortex.". Cell. 146 (1): 18–36. PMC 3610574. PMID 21729779. doi:10.1016/j.cell.2011.06.030.
- 12. Rash, BG; Ackman, JB; Rakic, P (February 2016). "Bidirectional radial Ca(2+) activity regulates neurogenesis and migration during early cortical column formation.". Science advances. 2 (2): e1501733. PMC 4771444. PMID 26933693. doi:10.1126/sciadv.1501733.
- Trepat, X. , et al. : Universal physical responses to stretch in the living cell. Nature 447(7144), 592 595 (2007)
- Jakkaraju, S. , Zhe, X. , Schuger, L. : Role of stretch in activation of smooth muscle cell lineage. Trends Cardiovasc. Med. 13(8), 330 335 (2003)
- Serena, E. , et al. : Electrical stimulation of human embryonic stem cells: cardiac differentiation and the generation of reactive oxygen species. Exp. Cell Res. 315(20), 3611 3619 (2009)
- Yamada, M. , et al. : Electrical stimulation modulates fate determination of differentiating embryonic stem cells. Stem Cells 25(3), 562 570 (2007)
زیرنویس
- ^ Zygote