معادله آرنیوس
معادله آرنیوس فرمولی برای وابستگی نرخ واکنش شیمیایی به دما میباشد. این فرمول توسط سوانت آرنیوس در سال ۱۸۸۹ پیشنهاد شد. این فرمول کاربردهای وسیع و مهمی را درتعیین نرخ واکنشهای شیمیایی و محاسبه انرژی فعال سازی دارد. آرنیوس توجیه فیزیکی و تفسیر برای فرمول ارائه داد.[1][2][3] در حال حاضر، این رابطه به عنوان یک رابطه تجربی شناخته میشود.[4]
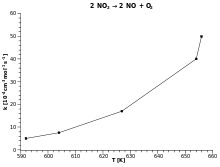
پلات K - T
معادله آرنیوس en:Arrhenius equation
جایی که:
پانویس
- Arrhenius, S.A. (1889). "Über die Dissociationswärme und den Einflusß der Temperatur auf den Dissociationsgrad der Elektrolyte". Z. Phys. Chem. 4: 96–116.
- Arrhenius, S.A. (1889). "Über die Reaktionsgeschwindigkeit bei der Inversion von Rohrzucker durch Säuren". ibid. 4: 226–248.
- Laidler, K. J. (1987) Chemical Kinetics,Third Edition, Harper & Row, p.42
- Kenneth Connors, Chemical Kinetics, 1990, VCH Publishers
- Arrhenius, S.A. (1889). "Über die Dissociationswärme und den Einflusß der Temperatur auf den Dissociationsgrad der Elektrolyte". Z. Phys. Chem. 4: 96–116.
- Arrhenius, S.A. (1889). "Über die Reaktionsgeschwindigkeit bei der Inversion von Rohrzucker durch Säuren". ibid. 4: 226–248.
- Laidler, K. J. (1987) Chemical Kinetics,Third Edition, Harper & Row, p.42
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.