شیکونین
شیکونین (به انگلیسی: shikonin) یک متابولیت ثانویه گیاهی است که دارای خواص داروئی قابل توجهی از جمله اثر ضد سرطان، ضد میکروب، ضد التهاب، بهبود زخم و ضد دیابت است.[1] شیکونین و مشتقات آن رنگدانههای قرمز رنگ از گروه نفتوکوئینونها هستند که در ریشه بسیاری از گونههای خانواده بوراژیناسه (Boraginaceae) شامل erythrorhizon ,Lithospermum Arnebia ,Onosma ,Alkanna ,Anchusa و Echium تجمع مییابند.[2] از آنجا که محل تجمع این رنگیزهها در بخش پوست ریشه میباشد، ریشههای این گیاهان به رنگ قرمز بنفش است. اگر شیکونین از بافتهای تازه استخراج شود، به تدریج طی چند روز تیره میشود و در نهایت تبدیل به رسوب سیاهی میگردد که تصور میشود پلیمر باشند.[3] خانواده بوراژیناسه اغلب گیاهان علفی چند ساله هستند و شامل حدود ۱۰۰ جنس و ۲۰۰۰ گونه است که در مناطق معتدل و گرمسیری توزیع شدهاند. متابولیتهای ثانویه مهم این خانواده آلکالوئیدها، نفتوکوئینونها، پلی فنولها، فیتواسترولها، ترپنوئیدها و اسیدهای چرب میباشد.[4] بهطورکلی متابولیتهای ثانویه گیاهان به سه گروه اصلی پلی فنولها، آلکالوئیدها و ترپنها دستهبندی میشوند. نفتوکوئینونها متعلق به دسته پلی فنولها میباشند که شیکونین و مشتقهای آن دارای بیشترین اهمیت تجاری در بین رنگدانههای نفتوکوئینون هستند.[2] شیکونین دارای خاصیت چربی دوستی بالایی است و در درجه حرارت بالا ناپایدار میباشد و تمایل به اکسید شدن و پلی مریزه شدن دارد.[5]

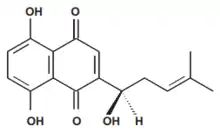
از مشتقهای مهم شیکونین میتوان دئوکسی شیکونین و استیل شیکونین را نام برد که دئوکسی شیکونین، فاقد عامل هیدروکسیل در زنجیره جانبی است و پیش ساز استیل شیکونین نیز میباشد.[3]
تاریخچه
استفاده از داروهای گیاهی و ترکیبهای طبیعی فرصتهای امیدوار کننده ای را برای درمان بیماریها و همچنین بکارگیری آنها به عنوان عوامل کمکی در شیمی درمانی برای بیماران سرطانی فراهم کردهاست. امروزه طب مکمل و جایگزین نظیر Traditional Chinese Medicine) TCM) بهطور گستردهای در سرتاسر جهان شناخته شدهاست. شیکونین یکی از ترکیبهای مهم طب سنتی چینی میباشد که اثرهای زیستی و دارویی آن به خوبی شناخته شدهاست.[6] ساختار شیمیایی شیکونین، اولین بار در سال ۱۹۱۸ پیشنهاد شد و سرانجام مشخص شد که این ترکیب ایزومر نوری آلکانین میباشد.[3] مشتق استیل شیکونین برای اولین بار در سال ۱۹۲۲ توسط کورودا و ماجیما از ریشههای اریترورایزن استخراج گردید. این شیمیدانها سپس مشتقهای دیگر، از جمله شیکونین را نیز جداسازی کردند و بسیاری از خواص شیمیایی آنها را تعیین کردند.[5] اولین تولید موفقیتآمیز شیکونین و تعدادی از مشتقهای آن در سال ۱۹۷۴ توسط تاباتا و همکارانش از کالوسهای کشت شده به دست آمد.[7] در دهههای ۱۹۷۰ و ۱۹۸۰ تولید صنعتی شیکونین از طریق کشتهای سلولی erythrorhizon توسط شرکت پتروشیمی میتسویی (Mitsui) راه اندازی گردید که از محیط کشت M9 برای تولید مشتقهای شیکونین استفاده میشد.[3] امروزه نیز به منظور تولید صنعتی این ترکیبها، بیشتر از کشت سلولی استفاده میشود که البته کشت تار کشنده نیز رواج زیادی پیدا کردهاست.[8]
کاربردها و خواص درمانی
شیکونین به علت دارا بودن خواص ضد التهابی، در ترمیم زخم استفاده میشود. بطوریکه در طب سنتی چینی برای مدتهای طولانی از ریشه این گیاهان برای درمان سوختگیها، زخمهای مقعد، بواسیر و زخمهای پوستی استفاده میشود. امروزه نیز اثرهای ترمیم کنندگی آن در زخمهای روده ای و پوستی به اثبات رسیدهاست.[9]
شیکونین دارای اثرهای ضد سرطانی متفاوتی میباشد. به عنوان مثال این ماده داروئی میتواند فعالیتهای آنزیم توپوایزومراز که نقش مهمی در تنظیم DNA سلولهای سرطانی از جمله تکثیر، نوترکیبی و رونویسی دارد را مهار کند. افزایش بیان P53 و مهار گلیکولیز سلول سرطانی از طریق هدفگیری پیرووات کیناز M2 یا PKM2 از مکانیسمهای دیگر مرگ سلولهای سرطانی القا شده با شیکونین است. از آنجا که سلولهای سرطانی به شدت بر گلیکولیز متکی هستند و PKM2 آخرین آنزیم محدود کننده سرعت در گلیکولیز است، شیکونین به عنوان یک مهار کننده طبیعی PKM2 میتواند باعث سرکوب رشد سلولهای سرطانی از طریق مهار منبع اصلی تولید ATP شود. همچنین شیکونین با اثر بر متابولیسم سلولی، فعالیت خود را به صورت حساس کردن سلولهای مقاوم به شیمی درمانی انجام میدهد.[10]
یکی از جنبههای برجسته سلولهای سرطانی در مقایسه با سلولهای طبیعی، سطوح بالایی از گونههای فعال اکسیژن (ROS) میباشد. میزان بالای ROS در سلولهای سرطانی، در شروع و پیشرفت سرطان بسیار مهم است. با این حال، تولید ROS اضافی میتواند سمی باشد و باعث آسیبپذیری بیشتر سلولهای سرطانی به تخریب از طریق استرس اکسیداتیوی شود. استرس اکسیداتیو باعث ایجاد آپوپتوز سلول از طریق یک سری مسیرهای پایین دست، مانند استرس شبکه اندوپلاسمی (ER) و آبشار میتوکندری میشود؛ بنابراین دستکاری سطوح ROS در سلولهای سرطانی، راهی است که بتوان سلولهای سرطانی را بهطور انتخابی از بین برد.[11] بسیاری از اثرهای سمی شیکونین نیز بر روی سلولهای سرطانی از طریق افزایش تولید گونههای فعال اکسیژن (ROS) برای ایجاد آپوپتوز وابسته به کاسپاز است. همچنین شیکونین باعث تنظیم کاهشی بیان ماتریکس متالو پروتئیناز (MMP) با میانجی گری فاکتور کاپا B هسته ای (NF-kB) میشود که به این ترتیب باعث کاهش ویژگی تهاجمی و متاستاز تومور میگردد.[6] این ماده دارویی به عنوان یک عامل کمکی برای درمان سلولهای سرطانی ریه نیز معرفی شدهاست. شیکونین باعث القا آپوپتوز، نکروز و پیری سلولهای سرطانی از طریق افزایش بیان ژن سرکوبگر تومور P53 میگردد. همچنین آزمایشها نشان دادهاست که در حدود ۲۴ ساعت پس از القا شیکونین، سطوح P53، P16 و کاسپاز ۳ بهطور قابل توجهی افزایش مییابند و همزمان با این افزایش، انتشار سیتوکروم C از میتوکندری به سیتوزول نیز مشاهده گردید.[6]
اثر ضد دیابت شیکونین و تأثیرش بر متابولیسم گلوکز از طریق مکانیسمهای مهاری و سرکوب ژنهای چربی ساز در کبد و عوامل رونویسی چربی سازی در بافت چربی سفید اثبات شدهاست. شیکونین توانایی اتصال PPARγ و C / EBPα (مهمترین عوامل رونویسی آدیپوژنز) به توالیهای هدفشان در DNA را مهار میکند. همچنین این ترکیب با فعال سازی مسیر / WNT β –کاتنین، بیان PPARγ و C / EBPα را سرکوب کرده و از تجمع چربی درون سلولی جلوگیری میکند.
شیکونین جذب گلوکز را افزایش میدهد. در واقع شیکونین انتقال GLUT4 را از وزیکولهای درون سلولی به سطح سلول افزایش میدهد که این همان مکانیسم انتهایی است که توسط انسولین اما با یک سیگنال درون سلولی متفاوتی انجام میشود. با این مشاهدهها دانشمندان امیدوارند که این ماده دارای اثر سودمندی بر متابولیسم گلوکز داشته باشد که این موضوع روشهای جدیدی را برای درمان دیابت نوع ۲ فراهم میکند.[5]
از خواص دیگر شیکونین میتوان به اثرات ضد میکروبی، ضد قارچی، ضد ویروسی، ضد انگلی، ضد اکسیدانی نیز اشاره کرد.[5]
شیکونین دارای خاصیت چربی دوستی بالایی است به همین علت از این ترکیب در کرمها و پمادها استفاده میشود.[5] از آنجا که پوست ریشه گیاهان خانواده بوراژیناسه حاوی مقادیر زیادی رنگدانههای نفتئوکینون قرمز رنگ است، از زمانهای بسیار قدیم به عنوان رنگ نیز استفاده میشدهاست.[7]
بیوسنتز و ترشح شیکونین
آنزیمهای مهم در مسیر بیوسنتز شیکونین فنیل آلانین آمونیا لیاز (PAL) و ۳ هیدروکسیل-۳-متیل گلوتاریل-CoA-ردوکتاز (HMGR) میباشد که میزان بیان آنها نیز در سلولهای تولیدکننده شیکونین بالا است.[2]
مطالعههای میکروسکوپ الکترونی حاکی از آن است که سلولهای تولیدکننده شیکونین حاوی وزیکولهای مشتق شده از شبکه آندوپلاسمی اند. این وزیکولها احتمالاً با استفاده از یکسری مکانیسمهای ناشناخته از غشای پلاسمایی عبور میکنند و شیکونین به صورت دانههای قرمز بر روی دیوارههای سلولی تجمع مییابد. از آنجا که مشتقات شیکونین بسیار آبگریز هستند، این وزیکولهای داخل سلولی مشابه چربیهای بدن به صورت تک لایههای چربی وجود دارند.[7]
منابع
- Sut S. , Pavela R. (2017). Identification of Onosma visianii Roots Extract and Purified Shikonin Derivatives as Potential Acaricidal Agents against Tetranychus urticae. Molecules.
- Malic S. , Bhushan Sh. , Sharma M and ahuja PS. (2016). Biotechnological approaches to the production of shikonins: a critical review with recent updates. Crit Rev Biotechnol. 36:327-40.
- Kazufumi Y. (2017). Lithospermum erythrorhizon cell cultures: Present and future aspects. Plant Biotechnology 34: 131–142.
- Mohammadi N. , Bahrami Gh. , Ghiasvand N. , Miraghaei Sh. , Madani S-H. , Karimi I. , Shokoohinia Y. (2017). The Wound Healing Effect of Various Extracts from Onosma Microcarpum Root in a Diabetic Animal Model. Reports in Pharmaceutical Sciences. 6: 59-67.
- Andújar I. , Ríos J.L. , Giner RM. , Recio MC.)2013b(. Pharmacological properties of shikonin -a review of literature since 2002. Planta Med. 79:1685–97.
- Yeh Y.C. , Liu T.J. , Lai H.C. (2015). Shikonin induces apoptosis, necrosis, and premature senescence of human A549 lung cancer cells through Upregulation of p53 Expression. Evid Based Complement Alternat Med 2015: 620383
- Yazaki K. , Matsuoka H. , Ujihara T. , Sato F. (1999). Shikonin biosynthesis in Lithospermum erythrorhizon: light-induced negative regulation of secondary metabolism. Plant Biotechnology. 16: 335-342.
- Chaudhury A. , Pal M. (2010) Induction of shikonin production in hairy root cultures of Arnebia hispididdima via Agrobacterium rhizogenes-mediated genetic transformation. J Crop Sci Biotech 13:99–106.
- Andújar I. , Rios J.L. , Giner R.M. , Recio M.C.)2013a(. Shikonin promotes intestinal wound healing in vitro via induction of TGF-β release in IEC-18 cells. Pharmaceutical Sciences. 49: 637–641.
- Li W. , Liu J. , Jackson K. , Shi R. , Zhao Y. (2014). Sensitizing the therapeutic efficacy of taxol with shikonin in human breast cancer cells. PloS one. 9: e94079.
- He G. , He G. , Zhou R. , Pi Z. , Zhu T. , Jiang L.)2016(. Enhancement of Cisplatin-Induced Colon Cancer Cells Apoptosis by Shikonin, a Natural Inducer of Ros in Vitro and in Vivo. Biochem Biophys Res Commun. 469:1075-1082.