طیفنگاری کارکردی فروسرخ نزدیک
طیفسنجی عملکردی فروسرخ نزدیک (به انگلیسی: functional Near InfraRed Spectroscopic) یک تکنیک مانیتورینگ نوری مغز است که از طیفسنجی نزدیک فروسرخ به منظور تصویربرداری عصبی عملکردی استفاده میکند.[1] با استفاده ازfNIRS، فعالیت مغز به کمک نور فروسرخ نزدیک برای تخمین فعالیت همودینامیکی قشر مغز که در پاسخ به فعالیت عصبی رخ میدهد، اندازهگیری میشود. در کنارEEG, fNIRS یکی از رایجترین روشهای تصویربرداری عصبی غیرتهاجمی است که میتواند به صورت قابلحمل استفاده شود. این سیگنال اغلب با سیگنال BOLD که توسط fMRI اندازهگیری میشود مقایسه میشود و قادر به اندازهگیری تغییرات غلظت اکسی هموگلوبین و دی اکسی هموگلوبین است،[2] اما فقط میتواند از مناطق نزدیک به کورتکس اندازهگیری کند. fNIRS همچنین ممکن است به عنوان توپوگرافی نوری شناخته شود و گاهی اوقات به سادگی با نام NIRS شناخته میشود.


شرح

fNIRS غلظت هموگلوبین را به واسطه تغییرات میزان جذب نور فروسرخ نزدیک تخمین میزند. هنگامی که نور از سر عبور میکند، بهطور متناوب توسط بافتی که از آن میگذرد، پراکنده میشود یا جذب میشود. از آنجا که هموگلوبین یک جذب کننده قابل توجه نور فروسرخ نزدیک است، میتوان از تغییرات میزان نور جذب شده برای اندازهگیری قابل اعتماد غلظت هموگلوبین استفاده کرد. تکنیکهای مختلف fNIRS همچنین میتوانند از روش انتشار نور برای تخمین حجم خون و اکسیژن رسانی استفاده کنند. این روش ایمن و غیرتهاجمی است و میتواند در کنار سایر روشهای تصویربرداری نیز مورد استفاده قرار گیرد.
fNIRS یک روش تصویربرداری غیرتهاجمی است که شامل کمی سازی غلظت کروموفور است. غلظت کروموفورها از اندازهگیری میرایی نور فروسرخ نزدیک یا تغییرات زمانی یا فازی به دست میآید. نور طیف fNIRS از مزیت پنجره نوری فروسرخ نزدیک (فاصله طیفی ۷۰۰–۹۰۰ نانومتر) استفاده میکند. در این پنجره نوری پوست، بافت و استخوان تقریباً شفاف هستند و هموگلوبین اکسیژنه (Hb) و هموگلوبین فاقد اکسیژن (deoxy-Hb) جذبکنندههای قوی این طیف نور هستند. این اصول اساسی از پالس اکسی مترها گرفته شدند.
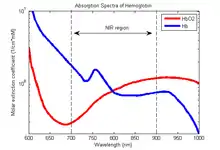
شش روش مختلف برای تعامل نور فروسرخ با بافت مغز وجود دارد: انتقال مستقیم، انتقال پراکنده، بازتاب منظم، بازتاب پراکنده، تفرق و جذب. fNIRS برپدیده جذب تمرکز دارد. طیف جذب هموگلوبین اکسیژنه و هموگلوبین فاقد اکسیژن متفاوت هستند. این پدیده اندازهگیری تغییرات نسبی غلظت هموگلوبین را به کمک خاصیت میرایی نور در طول موجهای مختلف فراهم میکند. دو یا چند طول موج انتخاب میشوند. یک طول موج بالاتر و دیگری زیر نقطه ایزوبستیک با طول موج ۸۱۰نانومتر (که در آن deoxy-Hb و oxy-Hb ضرایب جذب یکسان دارند)انتخاب میشوند. با استفاده از قانون بیر- لمبرت اصلاح شده، تغییرات نسبی غلظت میتواند به عنوان تابعی از کل طول مسیر طی شده فوتون محاسبه شود.[3]
بهطور معمول، ساطع کننده نور و آشکارسازهر دو بر یک طرف سطح جمجمه سوژه قرار میگیرند؛ بنابراین اندازهگیریهای ثبت شده از نور پراکنده برگشتی (منعکس شده) پس ازطی کردن مسیرهای بیضوی است.[4] fNIRS بیشترین حساسیت همودینامیکی را به تغییراتی که در نزدیکی پوست سر رخ میدهند دارد.[5] این آرتیفکتهای سطحی غالباً با استفاده از آشکارسازهای اضافی نور که در نزدیکی منبع نور قرار دارند، قابل تشخیص میشوند.[6]
قانون اصلاح شده بیر-لمبرت
قانون بیر-لامبرت (به انگلیسی: Beer-Lambert law) یکی از قوانین اصلی در طیفسنجی فوتومتری و اپتیک است. این قانون دربرگیرندهٔ ارتباط شدت نور جذبشده در اثر عبور از ماده همگن بدون پراکندگی با خصوصیات مواد میباشد. این قانون بهطور کلی به صورت زیر بیان میشود:
که در آن شدت نور اولیه، I شدت نور عبوری و A مقدار جذب[7] ماده است؛ که به صورت زیر تعریف میشود:
که در آن a ضریب جذب ماده (گاهی نیز با ε نشان داده میگردد)، b طول نمونه (ظرف نمونه) و c غلظت آن است.
تغییرات در شدت نور را میتوان به تغییر غلظت نسبی هموگلوبین از طریق قانون اصلاح شده بیر-لمبرت ربط داد. این روش همچنین برای تعیین اندازه تغییرات غلظت هموگلوبین، از تغییرات نسبی در میرایی نور و قانون بیر- لمبرت استفاده میکند.[8]
| اختصارات پایه (fNIRS)
BFi = blood flow index CBF = cerebral blood flow CBV = cerebral blood volume CMRO2= metabolic rate of oxygen CW= continuous wave DCS = diffuse correlation spectroscopy FD = frequency-domain Hb, HbR= deoxygenated hemoglobin HbO, HbO2= oxygenated hemoglobin HbT= total hemoglobin concentration HGB = blood hemoglobin SaO2= arterial saturation SO2= hemoglobin saturation SvO2= venous saturation TD=time-domain |
|---|
تاریخچه
آمریکا و بریتانیا
در سال ۱۹۷۷، جابسیس[9] گزارش داد که شفافیت بافت مغز در برابر نور فروسرخ نزدیک، یک روش غیرتهاجمی و مداوم را برای بررسی اشباع اکسیژن بافتی ممکن میسازد. Transillumination (پراکندگی در مسیر مستقیم) در بزرگسالان به دلیل میرایی نور از کاربرد محدودی برخوردار بود و به سرعت با تکنیکهای مبتنی بر حالت بازتاب جایگزین شد و در نتیجه سیستمهای NIRS به سرعت پیشرفت کردند. تا سال ۱۹۸۵، اولین مطالعات در مورد اکسیژن رسانی بافت کورتکس توسط ام. فراری انجام شد. در سال ۱۹۸۹، هاماماتسو با همکاری دیوید دلپی از دانشگاه کالج لندن، اولین سیستم تجاری NIRS را با نام NIR-1000 ساختند که یک دستگاه مانیتورینگ اکسیژن مغزی بود. روشهای NIRS در ابتدا برای اکسیژن سنجی مغزی در دهه ۱۹۹۰ استفاده شد. در سال ۱۹۹۳، چهار مقاله منتشر شد که امکانپذیری fnirs در انسان بالغ را نشان داد. تکنیکهای NIRS با کارهای دانشمندانی چون Randall Barbour , Britton Chance , Arno Villringer , M.Cope , D. T. Delpy , Enrico Gratton و دیگران گسترش یافت. در حال حاضر، fNIRS پوشیدنی در حال توسعه است.
ژاپن

در همین حال، در اواسط دهه ۸۰، محققان ژاپنی در آزمایشگاه تحقیقاتی مرکزی هیتاچی تصمیم گرفتند تا با استفاده ازرشته پالس متشکل از اشعههای ۷۰ پیکوثانیهای، یک سیستم مانیتورینگ مغزی مبتنی بر NIRS بسازند. این تلاش زمانی آشکار شد که این تیم، به همراه کارشناس برجسته خود، دکتر هیداکی کویزومی، یک سمپوزیوم را برای اعلام اصل "توپوگرافی نوری" در ژانویه ۱۹۹۵ برگزار کردند. در واقع، اصطلاح توپوگرافی نوری از مفهوم استفاده از نور در "نقشه برداری ۲ بعدی به همراه اطلاعات ۱ بعدی" یا توپوگرافی گرفته شدهاست. این ایده با موفقیت در راه اندازی اولین دستگاه fNIRS (یا همان توپوگرافی نوری) بر اساس حوزه فرکانس در سال ۲۰۰۱ اجرا شد: Hitachi ETG-100. بعداً، هارومی اویشی، دانشجوی دکترای دانشگاه ناگویا، رساله دکترای خود را در سال ۲۰۰۳ با موضوع "الگوهای فعالیت عصبی کورتکس در زبان آموزان با استفاده از ETG-100" زیر نظر پروفسور تورو کینوشیتا منتشر کرد و چشمانداز جدیدی در مورد استفاده از fNIRS ارائه کرد. این شرکت از آن زمان تاکنون سری ETG را گسترش دادهاست.
روشهای طیفسنجی
در حال حاضر، سه روش طیفسنجی کارکردی فروسرخ نزدیک وجود دارد:
- موج پیوسته
- حوزه فرکانس
- حوزه زمان
موج پیوسته
سیستم موج پیوسته از منابع نوری با فرکانس و دامنه ثابت استفاده میکند. در حقیقت، برای اندازهگیری تغییرات دقیق غلظت HbO با قانون بیر-لمبرت اصلاح شده، باید طول مسیر طی شده فوتون را بدانیم. با این حال، این سیستم هیچ اطلاعاتی از طول مسیر فوتون ارائه نمیدهد، بنابراین تغییرات در غلظت HbO نسبت به طول مسیر ناشناخته است. بسیاری از سیستمهای تجاری fnirs موج پیوسته، از تخمینهای طول مسیر فوتون حاصل از شبیهسازی رایانه ای مونت کارلو و مدلهای فیزیکی، برای تخمین تقریبی کمیت غلظت هموگلوبین استفاده میکنند.
که در این معادله OD چگالی نوری یا میرایی است. I0 شدت نور ساطع شدهاست و I شدت نور اندازهگیری شدهاست. ԑ ضریب میرایی و [X] غلظت کروموفومور است. l فاصله بین منبع و آشکارساز است و DPF فاکتور دیفرانسیلی طول مسیر است. و در نهایت G یک عامل هندسی مرتبط با پراکندگی است. هنگامی که ضریب میرایی ԑ را داشته باشیم. افت پراکندگی دائمی محاسبه میشود. در نتیجه محاسبات به حالت دیفرانسیلی در زمان حل میشوند و معادله به معادله زیر کاهش مییابد:
که d کل طول مسیر تصحیح شده فوتون است. با استفاده از یک سیستم دو طول موجی، اندازه غلظت HbO2 و Hb را میتوان از حل معادله ماتریسی زیر به دست آورد:[10]
fNIRS موج پیوسته به دلیل سادگی و مقرون به صرفه بودن، رایجترین شکل fNIRS است زیرا ارزانترین هزسنه ساخت را دارد، با کانالهای بیشتر قابل استفاده است و از وضوح زمانی بالایی برخوردار است. با این حال، تفاوت بین تغییرات جذب و پراکندگی را تشخیص نمیدهد و نمیتواند مقادیر جذب مطلق را اندازهگیری کند؛ این بدان معنی است که فقط به تغییر نسبی غلظت HbO حساس است. سادگی و مقرون به صرفه بودن دستگاههای مبتنی بر موج پیوسته برای تعدادی از کاربردهای بالینی مطلوبترین تکنیک است: مراقبت از نوزاد، سیستمهای نظارت بر بیمار، توموگرافی نوری منتشر و غیره. علاوه بر این، به لطف قابلیت جابجایی آن، سیستمهای موج پیوسته بیسیم توسعه یافتهاند که این امکان را ایجاد میکنند تا افراد در محیطهای سرپایی، بالینی و ورزشی تحت نظر قرار گیرند.[11][12][13]
حوزه فرکانس
سیستم حوزه فرکانس، شامل منابع لیزر فروسرخ نزدیک است که یک موج سینوسی با دامنه مدولهشده را در فرکانسهای نزدیک به ۱۰۰ مگاهرتز تولید میکند. این سیستم میرایی، تغییر فاز و متوسط طول مسیر نور عبوری از بافت را اندازهگیری میکند. سیستم چندمسافته، که بخشی از fNIRS حوزه فرکانس است، نسبت به تفاوت در رنگ پوست حساس نیست و بدون در نظر گرفتن تنوع سوژههای مورد بررسی، نتایج ثابت میدهد.
تغییرات دامنه و فاز سیگنال برگشتی پراکنده، امکان اندازهگیری ضرایب جذب و پراکندگی بافت را فراهم میکند، بنابراین دیگر نیازی به اطلاعات طول مسیر فوتون نخواهیم داشت. همچنین از ضرایب به دست آمده، تغییرات غلظت پارامترهای همودینامیک را تعیین میکنیم. به دلیل نیاز به لیزرهای مدوله شده و همچنین اندازهگیریهای فازی، دستگاههای مبتنی بر سیستم حوزه فرکانس از نظر فنی نسبت به دستگاههای مبتنی بر موج پیوسته، پیچیدهتر هستند. (بنابراین گرانتر و بسیار کمتر قابل حمل هستند) سیستم قادر به اندازهگیری مقدا مطلق غلظتهای HbO و HbR است.
حوزه زمان
سیستم حوزه زمان یک پالس کوتاه فروسرخ نزدیک با طول پالسی در مرتبه پیکو ثانیه (حدود 70 ps) تولید میکند. از طریق اندازهگیریهای زمان عبور، ممکن است با تقسیم زمان بهدستآمده بر سرعت نور، طول مسیر فوتون بهطور مستقیم به دست آید. اطلاعات مربوط به تغییرات همودینامیکی را میتوان در میرایی، زوال و مشخصات زمانی سیگنال برگشتی پراکنده یافت. برای این فناوری شمارش فوتون معرفی شده، به منظور حفظ خطی بودن ۱ فوتون برای هر ۱۰۰ پالس شمارش میکند. دسنگاهای fnirs خوزه زمان دارای سرعت نمونه برداری آهسته و همچنین تعداد طول موج محدودی هستند. به دلیل نیاز به دستگاه شمارش فوتون، تشخیص سرعت بالا و انتشار دهندههای پرسرعت، روشهای حل شده با زمان گرانترین و از نظر فنی پیچیدهتر هستند.
دستگاههای حوزه زمان کاملاً غیرمتحرک، اشغال کننده فضا، پیچیدهترین از نظر ساخت، پرهزینهترین، بزرگترین و سنگینترین هستند. اما با این وجود، بالاترین حساسیت به عمق را دارند و توانایی ارائه دقیقترین مقادیر پایه هموگلوبین و اکسیژن رسانی را دارند.
طیفسنجی همبستگی پراکنده
سیستمهای طیفسنجی همبستگی پراکنده از گرادیانهای موضعی در میرایی نور برای تعیین نسبت مطلق oxy-Hb و deoxy-Hb استفاده میکنند. با استفاده از یک اندازهگیری فضایی، سیستمهای طیفسنجی همبستگی پراکندهبرای انجام این محاسبه به طول مسیر فوتون نیاز ندارند، با این حال غلظتهای اندازهگیریشده از اکسی-هموگلوبین و دیاکسید-هموگلوبین وابسته به به ضریب ناشناخته پراکندگی در بافت است. این روش معمولاً در سیستمهای اکسی متری مغزی که شاخص اکسیژن بافت (TOI) یا شاخص اشباع بافت (TSI) را گزارش میدهند، استفاده میشود.[14]
طراحی سیستم
حداقل دو مدل متن باز fNIRS بصورت آنلاین در دسترس است:
نرم ازفراهای تجزیه و تحلیل دادهها
Homer3
HOMER3 به کاربران امکان میدهد تخمینها و نقشههای فعالیت مغزی را بدست آورند. این مجموعه ای از اسکریپتهای Matlab است که برای تجزیه و تحلیل دادههای fNIRS استفاده میشود. این مجموعه از اسکریپتها از اوایل دهه ۱۹۹۰ ابتدا به عنوان جعبه ابزار تصویربرداری حرکت فوتون به HOMER1 و HOMER2 و اکنون HOMER3 تکامل یافتهاند.[15]
جعبه ابزار NIRS
جدیدترین نرمافزار این حوزه است. این جعبه ابزار مجموعه ای از ابزارهای مبتنی بر Matlab برای تجزیه و تحلیل طیفسنجی عملکردی نزدیک فروسرخ (fNIRS) است. این جعبه ابزار فضای نام +nirs را تعریف میکند و شامل مجموعه ای از ابزارها برای پردازش سیگنال، نمایش و بررسی آماری دادههای fNIRS است. این جعبه ابزار حول یک چارچوب شی گرا از کلاسها و فضاهای نامی Matlab ساخته شدهاست.[16]
AtlasViewer
AtlasViewer اجازه میدهد دادههای fNIRS بر روی یک مدل از مغز تصویر شوند. علاوه بر این، همچنین به کاربر اجازه میدهد پروبهایی را طراحی کند که در نهایت میتوانند بر روی سر سوژه قرار گیرند.[17]
کاربرد
رابط مغز کامپیوتر
fNIRS با موفقیت به عنوان سیگنال کنترلی برای سیستمهای رابط مغز و کامپیوتر استفاده شدهاست.[18][19][20][21][22]
اتصالات کارکردی میان نواحی مغز
از اندازهگیری fNIRS میتوان برای شناخت اتصالات عملکردی مغز استفاده کرد. اندازهگیری fNIRS چند کاناله یک نقشه توپوگرافی از فعالیت عصبی ایجاد میکند. به موجب آن همبستگی زمانی بین وقایع مجزا از نظر مکانی میتواند تجزیه و تحلیل شود. اتصال عملکردی معمولاً همبستگی بین پاسخهای همودینامیک مناطق هدف را که از نظر مکانی مجزا هستند، در نظر گرفته میشود. در مطالعات مغزی، اندازهگیری اتصالات کارکردی معمولاً برای دادههای بیمار در حالت استراحت و همچنین دادههای ثبت شده در پارادایمهای تحریک انجام میشود. با توجه به هزینه کم، قابل حمل بودن و رزولوشن زمانی بالای fNIRS، در قیاس با fMRI، این روش در بعضی مطالعات مفیدتر است.[23]
اکسیمتری مغزی
مانیتورینگ NIRS از چند جهت مفید است. نوزادان نارس را میتوان تحت نظارت قرار داد تا هیپوکسی مغزی و هایپراکسی مغزی را با الگوهای مختلف فعالیت کاهش داد.[24] همچنین ای یک کمک مؤثر در ایجاد گذرگاه فرعی قلبی-ریوی است و برای بهبود نتایج بیمار و کاهش هزینهها و اقامت طولانی مدت به شدت توصیه میشود. استفاده از NIRS برای بیماران با آسیب مغزی نتایج غیرقطعی داشتهاست. به همین علت این کاربردها همچنان در حوزه تحقیقات باقی ماندهاند.
کلاه Fnirs
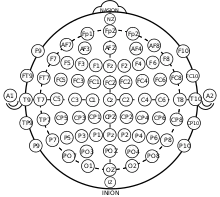
مکانها و نامهای الکترود fNIRS توسط سیستم بینالمللی ۱۰–۲۰ تعیین شدهاست. علاوه بر موقعیتهای استاندارد الکترودها، میتوان کانالهای تفکیک کوتاه را هم اضافه کرد. کانالهای تفکیک کوتاه امکان اندازهگیری سیگنالهای پوست سر را فراهم میکنند. از آنجا که کانالهای تفکیک کوتاه، سیگنال ناشی از پوست سر را اندازهگیری میکنند، سیگنال لایههای سطحی را که آرتیفکت محسوب میشوند را میتوان حذف کرد. در نتیجه پاسخ واقعی مغز را خواهیم داشت. آشکارسازهای کانال تفکیک کوتاه معمولاً ۸ میلیمتر دورتر از منبع قرار میگیرند. نیازی نیست که آنها در یک جهت خاص یا همجهت با منبع باشند.[25]
تصویربرداری عصبی کارکردی
استفاده از fNIRS به عنوان یک روش تصویربرداری عصبی عملکردی متکی به اصل همبستگی عصبی-عروقی است که با نام پاسخ همودینامیک یا پاسخ وابسته به سطح اکسیژن خون (BOLD) نیز شناخته میشود. این اصل همچنین هسته اصلی تکنیکهای fMRI را تشکیل میدهد. طبق این اصل، فعالیت عصبی یک ناحیه مغز با تغییرات مرتبط در جریان خون مغزی موضعی مرتبط است. fNIRS و fMRI به تغییرات فیزیولوژیکی مشابه حساس هستند و اغلب روشهای مقایسه ای هستند. مطالعات مربوط به fMRI و fNIRS نتایج بسیار همبستگی را در وظایف شناختی نشان میدهد.
مطالعات مربوط به fMRI و fNIRS نتایج بسیار نزدیکی را در وظایف شناختی نشان میدهند. fNIRS مزایای مختلفی در هزینه و قابلیت حمل نسبت به fMRI دارد، اما به دلیل محدودیت در قدرت گسیل کننده نور نمیتواند برای اندازهگیری فعالیت قشر بیش از ۴ سانتیمتر استفاده شود و دارای رزولوشن مکانی محدودتری است. fNIRS شامل استفاده از توموگرافی نوری منتشر برای اهداف کاربردی است. کانالهای fNIRS چندگانه میتوانند نقشههای عملکردی توپوگرافی دوبعدی از فعالیت مغز را فراهم کنند (به عنوان مثال با دستگاه هایHitachi ETG-4000، Artinis Oxymon , NIRx NIRScout). در حالی که برای ایجاد نقشههای توموگرافی سه بعدی میتوان از فاصلههای مختلف منابع نوری استفاده کرد.
هایپراسکنینگ
hyperscanning به معنی مانیتور کردن دو یا چند مغز به صورت همزمان است. با این روش همبستگی عصبی بین فردی (درون مغزی) در موقعیتهای مختلف اجتماعی بررسی میشود، که ثابت میکند fNIRS یک روش مناسب برای بررسی تعاملات اجتماعی زنده مغز به مغز است.[26]
مزایا و معایب
مزایای fNIRS در میان روشهای تصویربرداری مغز عبارتند از: غیرتهاجمی بودن، روشهای کم هزینه، ایمنی کامل، رزولوشن زمانی بالا، سازگاری کامل با سایر روشهای تصویربرداری و نشانگرهای متعدد زیستی همودینامیکی. با این حال، هیچ سیستمی بدون محدودیت نیست. برای fNIRS این موارد عبارتند از: حساسیت کم به فعالیتهای عصبی، تفکیک مکانی کم و عمق نفوذ کم.
مسیرهای اینده
علیرغم محدودیتهای اندک، دستگاههای fNIRS نسبتاً کوچک، سبک، قابل حمل و پوشیدنی هستند. با توجه به این ویژگیها، برنامههای کاربردی برای این دستگاهها حیرتآور است. این امر باعث میشود آنها در بسیاری از سناریوها به راحتی در دسترس باشند. به عنوان مثال، آنها توانایی استفاده در کلینیکها، پایش وضعیت کلی سلامت، یک محیط کاملاً طبیعی و به عنوان یک ردیاب سلامتی را دارند. در نهایت، افراد در معرض خطر در بیمارستانها میتوانند از مانیتورینگ عصبی و توانبخشی عصبی به کمک fNIRS، بهرهمند شوند. اکنون سیستمهای fNIRS تحقیقاتی کاملاً بیسیم در بازار وجود دارد.[31]
Fnirs در مقایسه با دیگر روشهای تصویربرداری عصبی
مقایسه تکنیکهای تصویربرداری عصبی نکته مهمی است که باید مورد توجه قرار گیرد. هنگام مقایسه این تکنیکها، مهم است که به رزولوشن زمانی، رزولوشن مکانی و درجه آزادی حرکت توجه کنیم. EEG (الکتروانسفالوگراف) و MEG (مگنتوآنسفالوگرافی) وضوح زمانی بالایی دارند، اما وضوح مکانی کمی دارند. EEG همچنین از درجه آزادی حرکت بالاتری از MEG برخوردار است. هنگام مشاهده fNIRS، در میابیم آنها شبیه EEG هستند. از تحرک و همچنین رزولوشن زمانی بالایی برخوردار هستند و از رزولوشن مکانی پایینی برخوردار هستند. اسکنهای PET و fMRIها با هم گروهبندی میشوند، با این حال تفاوت آنها با سایر اسکنهای تصویربرداری عصبی از همدیگر مجزا است. همه این اسکنهای تصویربرداری عصبی دارای ویژگیهای مهم و ارزشمند هستند که بسته به اهداف مورد نظر باید در موقعیت مناسب استفاده شوند. آنچه fNIRS را به عنوان یکی از موارد خاص تصویربرداری مورد توجه قرار میدهد سازگاری آن با برخی از این روشها از جمله: MRI , EEG و MEG است.
جستارهای وابسته
- علوم اعصاب شناختی[32]
- طیفشناسی فروسرخنزدیک
- Diffuse optical tomography[33]
- تصویربرداری عصبی کارکردی
پیوند به بیرون
منابع
- Ferrari, Marco; Quaresima, Valentina (2012). "A brief review on the history of human functional near-infrared spectroscopy (fNIRS) development and fields of application". NeuroImage. 63 (2): 921–935. doi:10.1016/j.neuroimage.2012.03.049. ISSN 1053-8119.
- Cui, Xu; Bray, Signe; Bryant, Daniel M.; Glover, Gary H.; Reiss, Allan L. (2011). "A quantitative comparison of NIRS and fMRI across multiple cognitive tasks". NeuroImage. 54 (4): 2808–2821. doi:10.1016/j.neuroimage.2010.10.069. ISSN 1053-8119. PMC 3021967.
- Villringer, A.; Chance, B. (1997). "Non-invasive optical spectroscopy and imaging of human brain function". Trends in Neurosciences. 20 (10): 435–442. doi:10.1016/S0166-2236(97)01132-6. PMID 9347608. S2CID 18077839.
- Li, Ting; Gong, Hui; Luo, Qingming (2011). "Visualization of light propagation in visible Chinese human head for functional near-infrared spectroscopy". Journal of Biomedical Optics. 16 (4): 045001. doi:10.1117/1.3567085. ISSN 1083-3668.
- Kohno, Satoru; Miyai, Ichiro; Seiyama, Akitoshi; Oda, Ichiro; Ishikawa, Akihiro; Tsuneishi, Shoichi; Amita, Takashi; Shimizu, Koji (2007). "Removal of the skin blood flow artifact in functional near-infrared spectroscopic imaging data through independent component analysis". Journal of Biomedical Optics. 12 (6): 062111. doi:10.1117/1.2814249. ISSN 1083-3668.
- Brigadoi, Sabrina; Cooper, Robert J. (2015). "How short is short? Optimum source–detector distance for short-separation channels in functional near-infrared spectroscopy". Neurophotonics. 2 (2): 025005. doi:10.1117/1.NPh.2.2.025005. ISSN 2329-423X. PMC 4478880.
- absorbance
- Modified Beer Lambert Law, retrieved 2020-03-26
- Jöbsis (1997). "Noninvasive, infrared monitoring of cerebral and myocardial oxygen sufficiency and circulatory parameters". Science. 198 (4323): 1264–1267. doi:10.1126/science.929199. PMID 929199.
- Ayaz, Hasan; Shewokis, Patricia A.; Curtin, Adrian; Izzetoglu, Meltem; Izzetoglu, Kurtulus; Onaral, Banu (2011). "Using MazeSuite and Functional Near Infrared Spectroscopy to Study Learning in Spatial Navigation". Journal of Visualized Experiments (56). doi:10.3791/3443. ISSN 1940-087X.
- Piper, Sophie K.; Krueger, Arne; Koch, Stefan P.; Mehnert, Jan; Habermehl, Christina; Steinbrink, Jens; Obrig, Hellmuth; Schmitz, Christoph H. (2014). "A wearable multi-channel fNIRS system for brain imaging in freely moving subjects". NeuroImage. 85: 64–71. doi:10.1016/j.neuroimage.2013.06.062. ISSN 1053-8119. PMC 3859838.
- Curtin, Adrian; Ayaz, Hasan (2018). "The Age of Neuroergonomics: Towards Ubiquitous and Continuous Measurement of Brain Function with fNIRS". Japanese Psychological Research. 60 (4): 374–386. doi:10.1111/jpr.12227. ISSN 0021-5368.
- Quaresima, Valentina; Ferrari, Marco (2016). "Functional Near-Infrared Spectroscopy (fNIRS) for Assessing Cerebral Cortex Function During Human Behavior in Natural/Social Situations: A Concise Review". Organizational Research Methods. 22 (1): 46–68. doi:10.1177/1094428116658959. ISSN 1094-4281.
- Ferrari, Marco (2007). "Progress of near-infrared spectroscopy and topography for brain and muscle clinical applications". Journal of Biomedical Optics. 12 (6): 062104. doi:10.1117/1.2804899. ISSN 1083-3668.
- "HOMER2". HOMER2. Retrieved 2019-11-26.
- Santosa, H. , Zhai, X. , Fishburn, F. , & Huppert, T. (2018). The NIRS Brain AnalyzIR Toolbox. Algorithms, 11(5), 73.
- Aasted, Christopher M.; Yücel, Meryem A.; Cooper, Robert J.; Dubb, Jay; Tsuzuki, Daisuke; Becerra, Lino; Petkov, Mike P.; Borsook, David; Dan, Ippeita; Boas, David A. (April 2015). "Anatomical guidance for functional near-infrared spectroscopy: AtlasViewer tutorial". Neurophotonics. 2 (2): 020801. doi:10.1117/1.NPh.2.2.020801. ISSN 2329-423X. PMC 4478785. PMID 26157991.
- Ayaz, H.; Shewokis, P. A.; Bunce, S.; Onaral, B. (2011). "An optical brain computer interface for environmental control". 2011 Annual International Conference of the IEEE Engineering in Medicine and Biology Society. p. 6327. doi:10.1109/IEMBS.2011.6091561. ISBN 978-1-4577-1589-1.
- Coyle, S. M.; Ward, T. S. E.; Markham, C. M. (2007). "Brain–computer interface using a simplified functional near-infrared spectroscopy system". Journal of Neural Engineering. 4 (3): 219–226. doi:10.1088/1741-2560/4/3/007. PMID 17873424.
- Sitaram, R.; Zhang, H.; Guan, C.; Thulasidas, M.; Hoshi, Y.; Ishikawa, A.; Shimizu, K.; Birbaumer, N. (2007). "Temporal classification of multichannel near-infrared spectroscopy signals of motor imagery for developing a brain–computer interface". NeuroImage. 34 (4): 1416–1427. doi:10.1016/j.neuroimage.2006.11.005. PMID 17196832.
- Naseer N.; Hong M.J.; Hong K. -S. (2014). "Online binary decision decoding using functional near-infrared spectroscopy for the development of brain-computer interface". Experimental Brain Research. 232 (2): 555–564. doi:10.1007/s00221-013-3764-1.
- Naseer N.; Hong K. -S. (2013). "Classification of functional near-infrared spectroscopy signals corresponding to the right- and left-wrist motor imagery for development of a brain-computer interfaces". Neuroscience Letters. 553: 84–89. doi:10.1016/j.neulet.2013.08.021.
- Nguyen, Thien; Babawale, Olajide; Kim, Tae; Jo, Hang Joon; Liu, Hanli; Kim, Jae Gwan (2018-11-01). "Exploring brain functional connectivity in rest and sleep states: a fNIRS study". Scientific Reports. 8 (1): 16144. Bibcode:2018NatSR...816144N. doi:10.1038/s41598-018-33439-2. ISSN 2045-2322. PMC 6212555. PMID 30385843.
- {{Rahimpour, A., Noubari, H. A., & Kazemian, M. (2018). A case-study of NIRS application for infant cerebral hemodynamic monitoring: A report of data analysis for feature extraction and infant classification into healthy and unhealthy. Informatics in Medicine Unlocked, 11, 44-50.}}
- Yücel, Meryem A.; Selb, Juliette; Aasted, Christopher M.; Petkov, Mike P.; Becerra, Lino; Borsook, David; Boas, David A. (July 2015). "Short separation regression improves statistical significance and better localizes the hemodynamic response obtained by near-infrared spectroscopy for tasks with differing autonomic responses". Neurophotonics. 2 (3): 035005. doi:10.1117/1.NPh.2.3.035005. ISSN 2329-423X. PMC 4717232. PMID 26835480.
- mari (2018-02-04). "fNIRS Hyperscanning: A door to real-world social neuroscience research". The Society for functional Near Infrared Spectroscopy. Retrieved 2020-03-26.
- "YouTube". www.youtube.com. Retrieved 2020-03-26.
- fNIRS of playing piano, retrieved 2020-03-26
- fNIRS of Observation, retrieved 2020-03-26
- fNIRS of Imagery, retrieved 2020-03-26
- Shin, Jaeyoung; Kwon, Jinuk; Choi, Jongkwan; Im, Chang-Hwan (2017-11-29). "Performance enhancement of a brain-computer interface using high-density multi-distance NIRS". Scientific Reports. 7 (1): 16545. Bibcode:2017NatSR...716545S. doi:10.1038/s41598-017-16639-0. ISSN 2045-2322. PMC 5707382. PMID 29185494.
- Yücel, Meryem A.; Selb, Juliette; Aasted, Christopher M.; Petkov, Mike P.; Becerra, Lino; Borsook, David; Boas, David A. (July 2015). "Short separation regression improves statistical significance and better localizes the hemodynamic response obtained by near-infrared spectroscopy for tasks with differing autonomic responses". Neurophotonics. 2 (3): 035005. doi:10.1117/1.NPh.2.3.035005. ISSN 2329-423X. PMC 4717232. PMID 26835480.
- "NIRx | fNIRS Systems | NIRS Devices". NIRx Medical Technologies. Retrieved 2019-11-26.