تثبیت کنندههای پلیمر
تثبیت کنندههای پلیمر (انگلیسی: polymer stabilizer ) افزودنی های شیمیایی هستند که ممکن است به مواد پلیمری مانند پلاستیک ها اضافه شوند تا تخریب آنها را مهار یا عقب اندازند. [1] فرآیندهای معمول تخریب پلیمر شامل اکسیداسیون ، آسیب اشعه ماورا بنفش، تخریب حرارتی ، ازونكافت ، ترکیباتي مانند فتواكسيداسيون ، و همچنین واکنش با بقایای کاتالیزور ، رنگ یا ناخالصی است. [2] همه این موارد پليمر را از طریق شكست زنجیرهي پليمري آن ، ترکیب مجدد کنترل نشده و اتصال عرضي ، از نظر شیمیایی تخریب می کنند ، که بر بسیاری از خصوصیات کلیدی مانند استحکام ، شكل پذیری ، ظاهر و رنگ تأثیر منفی می گذارد.
تثبیت کننده ها در تمام مراحل چرخه عمر پلیمر استفاده می شوند. آنها به محصولات پلاستیکی اجازه می دهند سریعتر و با نقص کمتری تولید شوند ، طول عمر مفید آنها را افزایش داده و بازیافت آنها را تسهیل کنند. با این حال آنها همچنین به تثبیت ضایعات پلاستیکي كمك ميكنند و باعث می شوند برای مدت بیشتری در محیط زيست باقی بمانند. انواع مختلفی از پلاستیکها وجود دارند و هر یک ممکن است در برابر چندین نوع تخریب آسیب پذیر باشد ، که معمولاً منجر به استفاده از چندین تثبیت کننده مختلف به صورت ترکیبی می شود. حتی برای اشیا ساخته شده از یک نوع پلاستیک ،کاربرد های مختلف ممکن است نیاز به تثبیت کنندههای مختلف داشته باشند. ملاحظات نظارتی ، مانند تأیید تماس با غذا نیز وجود دارد. بنابراین دامنه وسیعی از تثبیت کننده ها وجود دارد.
بازار تثبیت کننده های آنتی اکسیدانی برای سال 2017 ، 1.69 میلیارد دلار آمریکا تخمین زده شد [3] ، انتظار می رود که بازار کل برای تمام تثبیت کننده ها تا سال 2025 به 5.5 میلیارد دلار برسد. [4]
آنتی اکسیدان ها
آنتی اکسیدان ها مانع خوداکسیاشی که هنگام واکنش پلیمرها با اکسیژن اتمسفر اتفاق می افتد، می شوند. تخریب هوازی به تدریج در دمای اتاق اتفاق می افتد ، اما تقریباً تمام پلیمرها هنگام پردازش در دمای بالا در معرض خطر اکسیداسیون حرارتی قرار دارند. در قالبگیری یا ریخته گری پلاستیک ها (به عنوان مثال قالبگیری تزریقی ) نیاز است که پلاستیک بالاتر از نقطه ذوب یا دمای انتقال شیشه (حدود 200 تا 300 درجه سانتیگراد) باشند. در این شرایط واکنش با اکسیژن بسیار سریعتر اتفاق می افتد. پس از شروع فرایند ، خوداکسایش می تواند خودکاتالیزی باشد. [5] با این وجود، حتی با اینکه معمولاً تلاش می شود سطح اکسیژن کاهش یابد ، حذف کامل آن غالباً غیرقابل دستیابی است و حتی غلظت بسیار کم اکسیژن نیز می تواند برای شروع تخریب کافی باشد. حساسیت به اکسیداسیون بسته به نوع پلیمر مورد نظر به میزان قابل توجهی متفاوت است. بدون تثبیت کننده ها، پلی پروپیلن و پلیمرهای غیر اشباع مانند لاستیک طبیعی در دمای اتاق به آرامی تخریب می شوند ، در صورتی که پلیاستایرن حتی در دمای بالا نیز می تواند پایدار باشد. [6] آنتی اکسیدان ها در مرحله فرآوری از اهمیت زیادی برخوردار هستند ، به صورت تامین ثبات طولانی مدت در دمای محیط به طور فزاینده توسط تثبیت کننده های نور آمین (HALs). آنتی اکسیدان ها اغلب بسته به مکانیسم عملکردشان اولیه یا ثانویه خوانده می شوند.
آنتی اکسیدان های اولیه (باز دارنده های رادیکال)
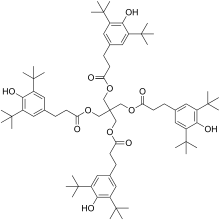
آنتی اکسیدان های اولیه (همچنین به آنتی اکسیدان های شکننده زنجیره شناخته می شوند) به عنوان بازدارنده های رادیکال عمل می کنند و رادیکال های پراکسی (ROO •) را ، و تا حد کمتری رادیکال های آلکوکسی (RO •) ، رادیکال های هیدروکسیل (HO •) و رادیکال های آلکیل (R • ) را حذف میکنند .اکسیداسیون با تشکیل رادیکال های آلکیل آغاز می شود ، وقتی دمای بالا و تنش برشی زیاد ناشی از فرآیند باعث شکست زنجیره های پلیمری به صورت همکافت میشود . این رادیکالهای آلکیل به سرعت با اکسیژن مولکولی واکنش نشان داده (ثابت سرعت ≈ 107–109 mol–1 s–1) تا رادیکال پراکسی تولید شود، [7] با تبدیل هیدروژن جدا شده از یک بخش پلیمر تازه در یک گام پخش زنجیره ای، رادیکالهای آلکیل جدید بدست میآید. [8] [9] روند کلی بسیار پیچیده است و بین پلیمرها متفاوت خواهد بود [10] اما چند مرحله ابتدایی به طور کلی به صورت زیر میباشد:
- RR → 2 R •
- R • + O 2 → ROO •
- ROO • + RH → ROOH + R •
به دلیل واکنش سریع رادیکال آلکیل اولیه (R •) با اکسیژن، مهار آن دشوار است و تنها با استفاده از آنتی اکسیدان های مخصوص پاک میشود [11] اکثر آنتی اکسیدان های اولیه به جای واکنش با رادیکالهای آلکیل اولیه با رادیکال های پراکسی ماندگارتر (ROO •) واکنش نشان می دهند. جدایش اتم هیدروژن معمولاً مرحله تعیین کننده سرعت تخریب پلیمر است و رادیکالهای پراکسی می توانند با اهدای هیدروژن از یک منبع جایگزین ، یعنی آنتی اکسیدان اصلی ، از بین بروند. این کار آنها را به هیدروپراکسید آلی (ROOH) تبدیل می کند. مهمترین تثبیت کننده تجاری برای اینکار فنول های محدود شده مانند BHT و آمین های معطر ثانویه مانند دیفنیلآمین هستند . آمین ها به طور معمول موثرتر هستند ، اما باعث تغییر رنگ مشخص می شوند ، که اغلب نامطلوب است (به عنوان مثال ، در بسته بندی مواد غذایی ، لباس). واکنش کلی با فنل ها در زیر نشان داده شده است:
- ROO• + ArOH → ROOH + ArO•
- ArO• → محصولات غیر رادیکال
محصولات نهایی از این واکنش ها به طور معمول کونین متید ها هستند که ممکن است انتقال ناخواسته رنگ داشته باشند.[12] اکسیدان های فنلی مدرن ساختار مولکولی پیچیدهای دارند، اغلب دارای یک گروه پروپیونات در موقعیت پارای فنل هستند.[13] کونین متیدهای اینها می توانند مجدد چیده شده و گروه فنلی آنتی اکسیدان را بازسازی کنند و اجازه دهند رادیکال های بیشتری از بین بروند.[14][15] در نهایت , آنتی اکسیدان های اولیه مصرف شونده بوده و هنگامی که آنها به طور کامل مصرف شوند پلیمر شروع به تخریب می کند.
آنتی اکسیدان های ثانویه (هیدروپراکسیدهای پاک کننده)
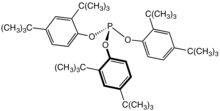
آنتی اکسیدان های ثانویه برای از بین بردن هیدروپراکسیدهای آلی (ROOH) تشکیل شده توسط اثر آنتی اکسیدان های اولیه عمل می کنند. واکنش پذیری هیدروپراکسیدها نسبت به گونه های رادیکال کمتر است اما می توانند واکنش های رادیکال تازه ای را شروع کند: [5]
- ROOH + RH → RO • + R • + H 2 O
از آنجا که فعالیت شیمیایی کمتری دارند ، به یک آنتی اکسیدان واکنش پذیرتر نیاز دارند. معمولاً دسته استفاده شده فسفیت استرها است( اغلب از فنل های محدود شده مانند تریس (2،4-دی-ترت بوتیل فنیل)فسفیت) . [16] این موارد هیدروپراکسیدهای پلیمر را به الکل تبدیل می کنند و در این فرآیند اکسیده شده و به ارگانوفسفات ها تبدیل می شوند: [17] [18]
- ROOH + P (OR ') 3 → OP (OR') 3 + ROH
سپس می توان تبادل استری را انجام داد که در آن پلیمر هیدروکسیله با یک فنول مبادله می شود: [19]
- ROH + OP (OR ') 3 → R'OH + OP (OR') 2 OR
این تبادل با آزاد سازی یک آنتی اکسیدان اولیه باعث تثبیت بیشتر پلیمر می شود ، به این دلیل است که فسفیت ها گاهی اوقات آنتی اکسیدان های چند منظوره محسوب می شوند زیرا می توانند هر دو نوع فعالیت را با هم ترکیب کنند و انجام دهند. ترکیبات آلی گوگرد همچنین تجزیه کننده های هیدروپراکسید کارآمدی هستند ، به طوری که تیواترها در برابر فرسایش حرارتی طولانی مدت به صورت ویژهای موثر هستند ، در نهایت تا سولفوکسیدها و سولفون ها اکسید می شوند. [20]
ضد ازونده
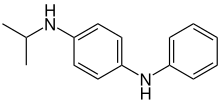
ضد ازونده ها از تخریب مواد ناشی از ازون جلوگیری و یا آنرا کند می کنند. این به طور طبیعی در هوا با غلظت بسیار کم وجود دارد اما در برابر پلیمرهای غیر اشباع مانند لاستیک ، که باعث پاره شدن لایه ازون می شود ، به طور ویژه واکنش پذیری بالایی دارد. مکانیزم ازونکافت با سایر اشکال اکسیداسیون متفاوت است و از این رو به طبقه خاص تثبیت کننده های آنتی اکسیدان خود نیاز دارد. این مواد اساساً بر پایه پارا-فنیلین دیآمین هستند و با واکنش سریعتر با ازون نسبت به گروههای عملکردی آسیب پذیر در پلیمر (به طور معمول گروههای آلکن) کار می کنند. آنها با داشتن انرژی یونش کم به این هدف دست می یابند که به آنها امکان می دهد از طریق انتقال الکترون با ازن واکنش نشان دهند و این آنها را به کاتیون های رادیکال تبدیل می کند که بوسیله خصلت آروماتیک تثبیت می شوند. چنین گونه هایی واکنش پذیر باقی می مانند و واکنش بیشتری نشان می دهند و محصولاتی مانند 1،4-بنزوکینون ، دایمرهای فنیلن دی آمین و رادیکال های آمینوکسیل می دهند . [21] [22] برخی از این محصولات می توانند توسط آنتی اکسیدان ها از بین بروند.
تثبیت کننده های نور
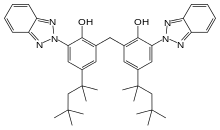
تثبیت کننده های نور برای جلوگیری از فتواکسیداسیون پلیمر استفاده می شود ، که نتیجه ترکیبی کنش نور و اکسیژن است. مانند خوداکسایش، این نیز یک فرآیند رادیکال آزاد است ، از این رو آنتی اکسیدان های توضیح داده شده در بالا عوامل مهار کننده موثری هستند ، با این حال دسته های دیگری از مواد افزودنی نیز مفید هستند ، مانند جاذب های UV ، سرد کننده های حالت برانگیخته و HALS. [23]
جاذب های اشعه ماورا بنفش
حساسیت به اشعه ماورا بنفش بین پلیمرهای مختلف به طور قابل توجهی متفاوت است. برخی از پلی کربنات ها ، پلی استرها و پلی اورتان ها بسیار حساس هستند ، و از طریق بازآرایی فریس تخریب می شوند. تثبیت کننده های ماورا بنفش به طور معمول با انتقال پروتون درون مولکولی برگشت پذیر انرژی اشعه ماورا بنفش را به عنوان گرما جذب و پراکنده می کنند. این امر باعث کاهش جذب اشعه ماورا بنفش توسط ماتریس پلیمر می شود و از این رو میزان هوازدگی(فرسایش در اثر هوا) را کاهش می دهد. بنزوتریازول ها و هیدروکسی فنیل تریازین ها(مانند بموتریزینول ) برای ایجاد ثبات پلی کربنات و آکریلیک ها استفاده می شوند ، [24] اوکسینیلید ها برای پلی آمید و پلی یورتان ها استفاده می شوند، در حالی که بنزوفنون ها برای پی وی سی استفاده می شوند .
سولفید پلی فنیلن به شدت جذب نور بوده و تثبیت آن دشوار است. حتی آنتی اکسیدان ها در این پلیمر غنی از الکترون از کار باز می مانند. اسیدها یا بازهای موجود در ماتریس سولفید پلی فنیلن می توانند عملکرد جاذب های متداول اشعه فرا بنفش مانند HPBT را مختل کنند. PTHPBT ، که یک نوع اصلاح شده HPBT است ، حتی در این شرایط نیز موثر است. [25]
سردکننده های ناگهانی
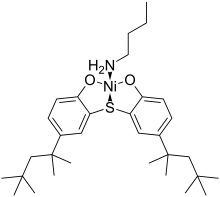
فتواکسیداسیون می تواند با جذب نور توسط یک رنگبر درون پلیمر (که ممکن است یک رنگ یا ناخالصی باشد) شروع شود و باعث ورود آن به حالت برانگیخته شود . سپس این پلیمر می تواند با اکسیژن محیط واکنش داده و آن را به اکسیژن تک اتمی واکنش پذیر تبدیل کند. سرد کننده ها قادرند انرژی را از طریق مکانیزم انتقال انرژی رزونانسی فورستر از مولکولهای برانگیخته جذب کرده و سپس آن را به صورت نور فلورسنت با فرکانس پایین و یا گرما ، بی خطر پراکنده کنند. اکسیژن تک اتمی را می توان توسط کلاته ای فلزی سرد کرد ، فنول های نیکل یک نمونه متدوال است. [26]
تثبیت کننده های نور آمین محدود شده
S-1_100.svg.png.webp)
توانایی تثبیت کننده های نور آمین محدود شده (HALS یا HAS) برای پاکسازی رادیکال های تولید شده در اثر هوازدگی ، از طریق تشکیل رادیکال های آمینوکسیل از طریق فرآیندی معروف به چرخه دنیسوف قابل توضیح است. رادیکال آمینوکسیل (NO •) با رادیکال های آزاد در پلیمرها ترکیب می شود:
N-O• + R• → N-O-R
اگرچه به طور معمول به عنوان تثبیت کننده نور در نظر گرفته می شوند ، اما می توانند تخریب گرمایی را نیز تثبیت کنند.
با اینکه HALS در پلی الفین ها ، پلی اتیلن و پلی اورتان بسیار موثر است ، در پلی وینیل کلراید (PVC) بی اثر هستند. تصور می شود که توانایی آنها در تشکیل رادیکال های نیتروکسیل مختل شده است. HALS به عنوان یک پایه عمل می کند و توسط هیدروکلریدریک اسید (HCl) که از فتواکسیداسیون PVC آزاد می شود خنثی می شود. NOR HALS که اخیراً ساخته شده است استثنا می باشد ، که یک پایه قوی نیست و توسط HCl بی اثر نمی شود. [27]
دیگر دسته ها
پلیمرها توسط عواملل مختلف فراتر از اکسیژن و نور در معرض تخریب قرار دارند.
اسید پاککن ها
پاک کننده اسیدها که به آنتی اسیدها نیز شناخته می شوند ، ناخالصی های اسیدی را خنثی می کند ، خصوصاً مواردی که هیدروژن کلرید(HCl) آزاد می کنند. PVC به تخریب با اسید کاتالیز شده حساس است و این هیدروژن کلرید از خود پلیمر بدست می آید. کاتالیگرهای زیگلر-ناتا و بازدارنده های شعله هالوژنه نیز به عنوان منابع اسیدها عمل می کنند. بازدارنده های اسید رایج شامل صابون های فلزی مانند کلسیم استئارات ، مواد معدنی مانند هیدروتالاسیت و هیدروکلومیت و اکسیدهای فلزات پایهای مانند اکسید روی است .
غیر فعال کننده های فلزی
یونهای فلزی مانند یونهای Ti ، Al و Cu می توانند تخریب پلیمرها را تسریع کنند. [28] این مسئله در مواردی که پلیمرها در تماس مستقیم با فلز هستند ، مانند سیم کشی ها و کابل ها ، بسیار نگران کننده است. به طور کلی ، کاتالیزورهای فلزی مورد استفاده برای تشکیل پلیمر ممکن است در طول تولید به سادگی در آن محصور شوند ، این امر به طور معمول در مورد کاتالیزگرهای زیگلر-ناتا در پلی پروپیلن صادق است. در این موارد می توان غیر فعال کننده های فلزی برای بهبود پایداری اضافه کرد. غیرفعال کننده ها با تشکیل چنگالش کار می کنند تا یک مجموعه هماهنگی غیرفعال با یون فلز تشکیل دهند. ترکیبات زالن رایج است.
تثبیت کننده های گرما
تثبیت کننده های گرما (یا حرارت) بیشتر برای PVC استفاده می شوند ، زیرا مواد ناپایدار شده به طور خاص مستعد تخریب گرمایی هستند. این عوامل هیدروهالوژن زدایی را به حداقل می رسانند ، یک فرایند تخریب که از 70 درجه سانتیگراد شروع می شود. به محض شروع هیدروهالوژن زدایی، واکنش خودکاتالیزی می شود . از عوامل گوناگونی از جمله مشتقات فلزات سنگین (سرب ، کادمیوم) استفاده شده است. به طور فزاینده ای ، صابون های فلزی ("نمک" های فلزی اسیدهای چرب) ، گونه هایی مانند کلسیم استئارات ، مورد علاقه و توجه قرار می گیرند. [29] سطح افزودن معمولاً بین 2٪ تا 4٪ متفاوت است. انتخاب بهترین تثبیت کننده گرما به اثربخشی هزینه آن در استفاده نهایی ، الزامات مشخصات عملکردی ، فناوری ساخت و مصوبات نظارتی بستگی دارد.
بازدارنده های اشتعال
بازدارنده های شعله طیف گسترده ای از ترکیبات هستند که مقاومت پلیمرها در برابر آتش گرفتن را بهبود می بخشند. به عنوان مثال می توان به هیدروکسید آلومینیوم ، سنارمونتیت و ارگانوفسفاتهای مختلف اشاره کرد. [30] بازدارنده های شعله، کاهنده اثر آنتی اکسیدان ها شناخته می شوند. [31]
زیست کشها
تخریب حاصل از میکروارگانیسم ها ( زیستتجزیه پذیری ) شامل دسته خاص تثبیت کننده های زیستی و زیستکشهای خود است (به عنوان مثال ایزوتیازولینون ها ).
همچنین ببینید
- افزودنیهاي دیگر
منابع
- Zweifel, Hans; Maier, Ralph D.; Schiller, Michael (2009). Plastics additives handbook (6th ed.). Munich: Hanser. ISBN 978-3-446-40801-2.
- Singh, Baljit; Sharma, Nisha (March 2008). "Mechanistic implications of plastic degradation". Polymer Degradation and Stability. 93 (3): 561–584. doi:10.1016/j.polymdegradstab.2007.11.008.
- "Plastic antioxidants market projected to reach US$2.11 billion by 2022". Additives for Polymers. 2018 (2): 10. February 2018. doi:10.1016/S0306-3747(18)30046-0.
- "Ceresana analyses the market for polymer stabilizers". Additives for Polymers. 2019 (4): 11. April 2019. doi:10.1016/S0306-3747(19)30105-8.
- "Auto-Accelerated Oxidation of Plastics". Polymer Properties Database. Retrieved 22 January 2019.

- Geuskens, G.; Bastin, P.; Lu Vinh, Q.; Rens, M. (July 1981). "Photo-oxidation of polymers: Part IV—Influence of the processing conditions on the photo-oxidative stability of polystyrene". Polymer Degradation and Stability. 3 (4): 295–306. doi:10.1016/0141-3910(81)90025-2.
- Ingold, Keith U. (May 2002). "Peroxy radicals". Accounts of Chemical Research. 2 (1): 1–9. doi:10.1021/ar50013a001.
- Lucarini, Marco; Pedulli, Gian Franco (2010). "Free radical intermediates in the inhibition of the autoxidation reaction". Chemical Society Reviews. 39 (6): 2106–19. doi:10.1039/B901838G. PMID 20514720.
- Vulic, Ivan; Vitarelli, Giacomo; Zenner, John M. (January 2002). "Structure–property relationships: phenolic antioxidants with high efficiency and low colour contribution". Polymer Degradation and Stability. 78 (1): 27–34. doi:10.1016/S0141-3910(02)00115-5.
- Gryn'ova, Ganna; Hodgson, Jennifer L.; Coote, Michelle L. (2011). "Revising the mechanism of polymer autooxidation". Org. Biomol. Chem. 9 (2): 480–490. doi:10.1039/C0OB00596G. PMID 21072412.
- Yachigo, Shin'ichi; Sasaki, Manji; Ida, Kanako; Inoue, Kikumitsu; Tanaka, Shin'ya; Yoshiaki, Honda; Emiko, Fukuyo; Kazunori, Yanagi (January 1993). "Studies on polymer stabilizers: Part VI—Relationship between performance and molecular conformation". Polymer Degradation and Stability. 39 (3): 329–343. doi:10.1016/0141-3910(93)90009-8.
- Pospı́šil, J.; Habicher, W.-D.; Pilař, J.; Nešpůrek, S.; Kuthan, J.; Piringer, G.-O.; Zweifel, H. (January 2002). "Discoloration of polymers by phenolic antioxidants". Polymer Degradation and Stability. 77 (3): 531–538. doi:10.1016/S0141-3910(02)00112-X.
- Pospíšil, Jan (January 1988). "Mechanistic action of phenolic antioxidants in polymers—A review". Polymer Degradation and Stability. 20 (3–4): 181–202. doi:10.1016/0141-3910(88)90069-9.
- Gijsman, Pieter (2018). "Polymer Stabilization". Handbook of Environmental Degradation of Materials. pp. 369–395. doi:10.1016/B978-0-323-52472-8.00018-6. ISBN 978-0-323-52472-8.
- Pospíšil, Jan; Nešpůrek, Stanislav; Zweifel, Hans (October 1996). "The role of quinone methides in thermostabilization of hydrocarbon polymers—I. Formation and reactivity of quinone methides". Polymer Degradation and Stability. 54 (1): 7–14. doi:10.1016/0141-3910(96)00107-3.
- Wypych, George (2013). "Effect of Additives on Weathering". Handbook of Material Weathering. pp. 547–579. doi:10.1016/B978-1-895198-62-1.50018-4. ISBN 978-1-895198-62-1.
- Schwetlick, K. (1 January 1983). "Mechanisms of antioxidant action of organic phosphorus compounds". Pure and Applied Chemistry. 55 (10): 1629–1636. doi:10.1351/pac198355101629.
- Schwetlick, K.; König, T.; Rüger, C.; Pionteck, J.; Habicher, W.D. (January 1986). "Chain-breaking antioxidant activity of phosphite esters". Polymer Degradation and Stability. 15 (2): 97–108. doi:10.1016/0141-3910(86)90065-0.
- Schwetlick, Klaus; Habicher, Wolf D. (October 1995). "Organophosphorus antioxidants action mechanisms and new trends". Angewandte Makromolekulare Chemie. 232 (1): 239–246. doi:10.1002/apmc.1995.052320115.
- Kröhnke, C. (2016). "Polymer Stabilization". Reference Module in Materials Science and Materials Engineering. doi:10.1016/B978-0-12-803581-8.01487-9. ISBN 978-0-12-803581-8.
- Cataldo, Franco; Faucette, Brad; Huang, Semone; Ebenezer, Warren (January 2015). "On the early reaction stages of ozone with N,N′-substituted p-phenylenediamines (6PPD, 77PD) and N,N′,N"-substituted-1,3,5-triazine "Durazone®": An electron spin resonance (ESR) and electronic absorption spectroscopy study". Polymer Degradation and Stability. 111: 223–231. doi:10.1016/j.polymdegradstab.2014.11.011.
- Cataldo, Franco (January 2018). "Early stages of p-phenylenediamine antiozonants reaction with ozone: Radical cation and nitroxyl radical formation". Polymer Degradation and Stability. 147: 132–141. doi:10.1016/j.polymdegradstab.2017.11.020.
- Wiles, D.M.; Carlsson, D.J. (November 1980). "Photostabilisation mechanisms in polymers: A review". Polymer Degradation and Stability. 3 (1): 61–72. doi:10.1016/0141-3910(80)90008-7.
- Crawford, J (April 1999). "2(2-hydroxyphenyl)2H-benzotriazole ultraviolet stabilizers". Progress in Polymer Science. 24 (1): 7–43. doi:10.1016/S0079-6700(98)00012-4.
- Das, P.K.; DesLauriers, P.J.; Fahey, Darryl R.; Wood, F.K.; Cornforth, F.J. (January 1995). "Photostabilization of poly (p-phenylene sulfide)". Polymer Degradation and Stability. 48 (1): 1–10. doi:10.1016/0141-3910(95)00032-H.
- Zweig, A.; Henderson, W. A. (March 1975). "Singlet oxygen and polymer photooxidations. I. Sensitizers, quenchers, and reactants". Journal of Polymer Science: Polymer Chemistry Edition. 13 (3): 717–736. Bibcode:1975JPoSA..13..717Z. doi:10.1002/pol.1975.170130314.
- Capocci, Gerald; Hubbard, Mike (September 2005). "A radically new UV stabilizer for flexible PVC roofing membranes". Journal of Vinyl and Additive Technology. 11 (3): 91–94. doi:10.1002/vnl.20044.
- Osawa, Zenjiro (January 1988). "Role of metals and metal-deactivators in polymer degradation". Polymer Degradation and Stability. 20 (3–4): 203–236. doi:10.1016/0141-3910(88)90070-5.
- M. W. Allsopp, G. Vianello, "Poly(Vinyl Chloride)" in Ullmann's Encyclopedia of Industrial Chemistry, 2012, Wiley-VCH, Weinheim. doi:10.1002/14356007.a21_717.
- Camino, G.; Costa, L. (January 1988). "Performance and mechanisms of fire retardants in polymers—A review". Polymer Degradation and Stability. 20 (3–4): 271–294. doi:10.1016/0141-3910(88)90073-0.
- Pfaendner, Rudolf (December 2013). "(Photo)oxidative degradation and stabilization of flame retarded polymers". Polymer Degradation and Stability. 98 (12): 2430–2435. doi:10.1016/j.polymdegradstab.2013.07.005.