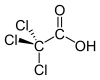
تری کلرواستیک اسید
اسید تری کلرواستیک اسید (به انگلیسی: Trichloro acetic acid (TCA)
| Trichloroacetic acid | |||
|---|---|---|---|
| |||
 | |||
Trichloroacetic acid | |||
| شناساگرها | |||
| شماره ثبت سیایاس | 76-03-9 | ||
| KEGG | C11150 | ||
| ChEMBL | CHEMBL14053 | ||
| شمارهٔ آرتیئیسیاس | AJ7875000 | ||
| جیمول-تصاویر سه بعدی | Image 1 | ||
SMILES
| |||
| خصوصیات | |||
| فرمول مولکولی | C2HCl3O2 | ||
| جرم مولی | ۱۶۳٫۳۹ g mol−1 | ||
| شکل ظاهری | White solid | ||
| چگالی | 1.63 g/cm³ | ||
| انحلالپذیری در آب | Soluble in 0.1 parts[1] | ||
| اسیدی (pKa) | 0.66[2] | ||
| ساختار | |||
| گشتاور دوقطبی | 3.23 D | ||
| خطرات | |||
| طبقهبندی ئییو | Corrosive (C) Dangerous for the environment (N) | ||
| کدهای ایمنی | R۳۵, R50/53 | ||
| شمارههای نگهداری | (S1/2), S26, S36/37/39, S45, S60, S61 | ||
| لوزی آتش | |||
| LD50 | 5000 mg/kg orally in rats[1] | ||
| ترکیبات مرتبط | |||
| مرتبط با کلرواستیک اسید | Chloroacetic acid دیکلرواستیک اسید | ||
| ترکیبات مرتبط | استیک اسید تریفلورواستیک اسید Tribromoacetic acid | ||
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |||
| | |||
| Infobox references | |||
|
| |||
رده درمانی: عوامل موضعی پوستی .
اشکال دارویی: محلول موضعی
تری کلرواستیک اسید که به تری کلرواتانوئیک اسید نیز معروف است. مشابه استیک اسید است که در آن سه اتم هیدروژن گروه متیل توسط اتم های کلر جایگزین شده اند. این ماده یک جامد کریستالی بی رنگ است که رطوبت هوا را جذب می کند و یک محلول غلیظ را تشکیل می دهد. محلول در آب است و این فرایند همراه با آزاد شدن گرما است. این ترکیب خورنده فلزات و بافت پارچه است. نمک ها و استرهای تری کلرواستریک اسید، تری کلرواستات نامیده می شوند.
روش تولید
- گزارش شده است که تری کلرواستیک اسید برای اولین بار در سال ۱۸۴۰ با کلره کردن استیک اسید در نور خورشید سنتز شد.
- این ماده در مقیاس صنعتی با کلره کردن استیک اسید یا کلرواستیک اسید در دمای ۱۴۰ تا ۱۶۰ درجه سانتی گراد تولید می شود. کلسیم هیپوکلریت ممکن است به عنوان یک شتاب دهنده کلرزنی اضافه شود و در بعضی موارد از کاتالیزورهای فلزی (مانند ترکیبات آهن یا مس) استفاده می شود. تری کلرواستیک اسید با تبلور از محصول خام جدا می شود.
- در واکنش کلر با استیک اسید در حضور کاتالیزور مناسب تهیه می شود.
CH۳COOH + 3Cl۲ → CCl۳COOH +3HCl
- مسیر دیگر تولید این ماده، اکسیداسیون تری کلرو استالدهید است.
کاربرد
این ماده در بیوشیمی به طور گسترده برای رسوب ماکرومولکول ها، از جمله پروتئین ها، DNA و RNA مورد استفاده قرار می گیرد. تری کلرواستیک اسید (TCA) و دی کلرواستیک اسید(DCA) هر دو در مواد آرایشی مانند لایه بردارهای شیمیایی، پاک کننده خالکوبی و همچنین به عنوان داروی موضعی برای درمان زگیل ها از جمله زگیل های تناسلی استفاده می شوند.
سدیم تری کلرواستات با خنثی کردن تری کلرواستریک اسید با محلول سدیم هیدروکسید یا سدیم کربنات بصورت صنعتی تولید می شود.
موارد مصرف
درمان زگیل (از جمله زگیل آنوژنیتال)، کک و مک، پیلینگ شیمیایی و برداشتن تاتو. این اسید در شیمی برای رسوب ماکرومولکولهایی مانند پروتئینها نیز به کار میرود
مکانیسم اثر
پیلینگ شیمیایی و از بین بردن سلولهای سطحی
عوارض جانبی
سوزش پوست
منابع
- Budavari, Susan, ed. (1996), The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (12th ed.), Merck, ISBN 0911910123
- Databog fysik kemi, F&K Forlaget 11. udgave 2009
- ویکیپدیای انگلیسی