جهش پذیرفته نقطهای
جهش پذیرفته نقطهای (Point accepted mutation یا PAM یا Percent Accepted Mutation) یک مجموعه از ماتریسها برای نمرهدهی به همترازی توالیها است. مارگارت دیهاف[1] ماتریس PAM را در سال ۱۹۷۸ بر مبنای ۱۵۷۲ جهش مشاهده شده در ۷۱ خانواده باپروتئنهای بسیار مرتبط معرفی کرد. [2] هر ماتریس در سطرها و ستونهای خود ۲۰ آمینو اسید دارد و هر درایه از ماتریس احتمال جایگزینی یک آمینو اسید با دیگری را مشخص میکند. این نوع ماتریسها را به طور کلی ماتریسهای جایگزینی مینامند.
این ماتریس در بیوانفورماتیک برای به دست آوردن ماتریس نمرهدهی جهت ارزیابی شباهت دو دنباله به کار میرود. برای مثال احتمال ۱۸ درصدی جایگزینی آرژنین با لیسین در این ماتریس امتیاز ۳ را به همراه خواهد داشت. در محاسبات فرکانس ظهور آمینو اسیدها و مقادیر احتمالات از روی دنبالههای شناخته شده به دست میآید.[3]
ماتریسهای PAM مفهوم مدل زنجیره مارکوف در جهش پروتئین را تداعی میکنند.[4][5] ماتریسهای PAM عادیسازی شدهاند، برای مثال ماتریس PAM۱ احتمال جایگزینیهایی را نشان میدهد که یک جهش نقطه در هر ۱۰۰ آمینو اسید را تجربه کردهاند. جهشها ممکن است همپوشانی داشته باشند، در ماتریس PAM۲۵۰ باید در هر ۱۰۰ آمینو اسید ۲۵۰ جهش دیده شود اما تاکنون ۸۰ جهش مؤثر دیده شدهاست.
پیش زمینه زیستی

دستورات ژنتیکی هر سلول خود تکثیر شونده درون یک اندامگان زنده درون دی ان ای آن قرار دارند.[6] در طول حیات سلول، این اطلاعات توسط مکانیسم های سلولی رونوشت میشوند تا پروتئین تولید شود و یا دستورات لازم برای سلول های دختر در هنگام تقسیم سلولی فراهم شود و در هنگام انجام این فرایند ها ممکن است دی ان ای تغییر کند.[6][7] به این تغییر جهش گفته میشود. در سطح سلولی، ساز و کار هایی نظارتی وجود دارد که اکثر - نه همه - این تغییر ها را قبل از تکثیر دی ان ای اصلاح می کند.[7][8]
یکی از جهش هایی که ممکن است در جایگزینی یک نوکلئوتید رخ دهد، جهش نقطه ای است. اگر یک جهش نقطه ای درون یک ناحیه بیان شده از ژن یا اگزون رخ دهد، رمز ژنتیکی مشخص کننده یک آمینو اسید خاص درون پروتئین تولید شده از روی ژن را تغییر خواهد داد.[7] با وجود افزونگی های رمز ژنتیکی، این امکان وجود دارد که این جهش آمینو اسید های تولید شده در زمان ترجمه را تغییر دهد و در نتیجه ساختار پروتئین تغییر کند.
عملکرد یک پروتئین به شدت به ساختار آن وابسته است.[9] تغییر تنها یک آمینو اسید درون پروتئین می تواند کارآمدی آن را کاهش دهد و یا حتی جهش می تواند عملکرد پروتئین را تغییر دهد.[7] اینگونه تغییرات میتوانند شدیدا میتوانند عملکرد های حیاتی سلول را تحت تاثیر قرار دهند به صورتی که پروتئین باعث میشود سلول، و در شرایط شدید تر کل اندامگان بمیرند.[10] در مقابل، تغییر ممکن است به سلول اجازه دهد که عملکرد خود را هرچند متفاوت ادامه دهد و جهش می تواند به فرزند آن اندامگان انتقال یابد. این احتمال وجود دارد که جهش درون جمعیت باقی بماند. همچنین این احتمال وجود دارد که این تغییرات در عملکرد ها مفید و سودمند باشند. در همه کدام از این حالت ها، در صورت شرکت در فرآیند انتخاب طبیعی، جهش های نقطه ای با موفقیت وارد خزانه ژنتیکی میشوند.
۲۰ نوع مختلف آمینو اسید که به وسیله کد ژنتیکی ترجمه میشوند تفاوت زیادی در ویژگی های فیزیکی و شیمیایی زنجیره کناری خود دارند.[9] البته این آمینو اسید ها میتوانند در گروه هایی با ویژگی های فیزیکی-شیمیایی مشابه گروه بندی شوند.[9] احتمال اینکه جایگزینی یک آمینو اسید با آمینو اسید دیگری از گروه خودش تاثیرات مشابهی روی ساختار و عملکرد یک پروتئین داشته باشد بیشتر از وقتی است که آن آمینو اسید با آمینو اسیدی از گروه دیگر جایگزین شود. در نتیجه پذیرش یک تغییر به عنوان جهش نقطه ای به شدت وابسته به آمینو اسید جایگزین کننده و آمینو اسید جایگزین شونده است. ماتریس های جهش پذیرفته نقطه ای (PAM) یک ابزار ریاضی برای محاسبه نرخ های متغیر پذیرش در هنگام سنجیدن شباهت پروتئین ها هنگام هم ترازی هستند.
واژه شناسی
در ابتدا عبارت جهش نقطه ای پذیرفته (به انگلیسی: accepted point mutation) برای توضیح پدیده جهش استفاده میشد. ولی عبارت مخفف PAM به دلیل خوانایی بیشتر به APM ترجیح داده شد بنابراین عبارت متناظر با آن یعنی جهش پذیرفته نقطه ای (به انگلیسی: point accepted mutation) معمولا استفاده میشود.[11] به دلیل اینکه مقدار در ماتریس بیانگر تعداد جهش ها در هر ۱۰۰ آمینو اسید است که می تواند با درصد عنوان شود، گاهی اوقات از عبارت درصد جهش پذیرفته استفاده میشود.
مهم است که بین جهش های پذیرفته نقطه ای (PAMs)، ماتریسهای جهش پذیرفته نقطه ای (PAM matrices) و ماتریس تمایز قائل شویم. عبارت 'جهش پذیرفته نقطه ای' به خود رویداد جهش اشاره می کند. اما عبارت 'ماتریسهای جهش پذیرفته نقطه ای' به یکی از ماتریس های خانواده ای از ماتریس ها اشاره می کند که حاوی امتیاز هایی هستند که نشان میدهد تا چه اندازه محتمل است که دو آمینو اسید طی یک توالی از رویداد های جهش با یکدیگر هم تراز شوند. ماتریس در واقع یک ماتریس جهش پذیرفته نقطه ای است که مربوط به بازه ای از زمان است که به اندازه کافی طولانی باشد تا جهش بتواند به ازای ۱۰۰ آمینو اسید رخ دهد.
ساخت ماتریس های PAM
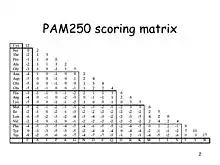
ماتریس های جهش پذیرفته نقطه ای (PAM) توسط مارگارت دایهوف در سال ۱۹۸۷ میلادی معرفی شدند.[12] شیوه محاسبه این ماتریس ها بر اساس مشاهده ۱۵۷۲ جهش در درخت تبارزایی ۷۱ خانواده پروتئین های بسیار مرتبط با یکدیگر بود. پروتئین های مورد مطالعه بر اساس داشتن شباهت زیاد با اجدادشان انتخاب شدند. چینش رشته پروتئین های انتخاب شده باید حداقل ۸۵٪ شباهت می داشتند.[11][13] در نتیجه معقول است که فرض کنیم که هرگونه عدم تطابق در چینش رشته پروتئین ها نتیجه یک رویداد جهش است و نه چند جهش در همان جایگاه در رشته پروتئین.
هر ماتریس PAM شامل ۲۰ سطر و ۲۰ ستون است که هر کدام از آنها نشان دهنده یکی از ۲۰ آمینو اسید ترجمه شده از رمز ژنتیکی هستند. مقدار هر سلول این ماتریس مربوط به احتمال هم تراز شدن آمینو اسید مربوط به آن سطر قبل از جهش با آمینو اسید مربوط به آن ستون بعد از جهش است.[11][12][13] بر اساس این تعریف، ماتریس های PAM نوعی ماتریس جایگزینی اند.
کاربرد ها
شناخت جهش پذیرفته تک نقطه ای و ماتریس های مرتبط به آن و همچنین شناخت ویژگی های این ماتریس ها کاربرد های بسیار وسیعی دارد. یکی از این کاربرد ها شناخت علل به وجود آمدن بسیاری از بیماری های مرتبط با دی ان ای و تغییر ژن ها است. امروزه به کمک این موارد، میدانیم که جهش در تنها یک عضو از پروتئین می تواند به تعداد زیادی از شرایط آسیب شناسی اجتماعی مرتبط باشد. به عنوان مثال آلزایمر، پارکینسون و بیماری کروتزفلد جاکوب. کیفیت و کمیت زیاد اطلاعات کنونی موجود در مورد چندریختی تک-نوکلئوتید ها به نرم افزار های یادگیری ماشین اجازه میدهد تا به وجود آمدن بیماری های انسانی به واسطه جهش پذیرفته تک نقطه ای را از قبل پیش بینی کنیم.[14]
نمونه های دیگر این کاربر در شناخت بیماری منکس[15]، بیماری گوشه[16]، بیماری های عروقی[17]، کمخونی داسی شکل[18] و بسیاری دیگر از بیماری ها قابل مشاهده است.
جستارهای وابسته
منابع
- Margaret Dayhoff
- Dayhoff, M.O., Schwartz, R. and Orcutt, B.C. (1978). "A model of Evolutionary Change in Proteins". Atlas of protein sequence and structure (volume 5, supplement 3 ed.). Nat. Biomed. Res. Found. pp. 345–358. ISBN 0912466073.
- Pevsner J (2009). "Pairwise Sequence Alignment". Bioinformatics and Functional Genomics (2nd ed.). Wiley-Blackwell. pp. 58–63. ISBN 978-0-470-08585-1.
- Kosiol C, Goldman N. (2005). "Different versions of the Dayhoff rate matrix". Molecular biology and evolution. 22 (2): 193–9. doi:10.1093/molbev/msi005. PMID 15483331. Archived from the original on 7 September 2008. Retrieved 28 June 2011.
- Liò P, Goldman N. (1998). "Models of molecular evolution and phylogeny". Genome research. 8 (12): 1233–44. doi:10.1101/gr.8.12.1233. PMID 9872979. Archived from the original on 27 July 2012. Retrieved 28 June 2011.
- Campbell NA, Reece JB, Meyers N; Urry LA; Cain ML; Wasserman SA; Minorsky PV; Jackson RB (2009). "The Molecular Basis of Inheritance". Biology: Australian Version (8th ed.). Pearson Education Australia. pp. 307–325. ISBN 9781442502215.
- Campbell NA, Reece JB, Meyers N; Urry LA; Cain ML; Wasserman SA; Minorsky PV; Jackson RB (2009). "The Molecular Basis of Inheritance". Biology: Australian Version (8th ed.). Pearson Education Australia. pp. 307–325. ISBN 9781442502215.
- Pal JK, Ghaskadbi SS (2009). "DNA Damage, Repair and Recombination". Fundamentals of Molecular Biology (1st ed.). Oxford University Press. pp. 187–203. ISBN 9780195697810.
- Campbell NA, Reece JB, Meyers N; Urry LA; Cain ML; Wasserman SA; Minorsky PV; Jackson RB (2009). "The Structure and Function of Large Biological Molecules". Biology: Australian Version (8th ed.). Pearson Education Australia. pp. 68–89. ISBN 9781442502215.
- Lobo, Ingrid (2008). "Mendelian Ratios and Lethal Genes". Nature. Retrieved 19 October 2013.
- Pevsner J (2009). "Pairwise Sequence Alignment". Bioinformatics and Functional Genomics (2nd ed.). Wiley-Blackwell. pp. 58–68. ISBN 978-0-470-08585-1.
- Dayhoff, M.O., Schwartz, R. and Orcutt, B.C. (1978). "A model of Evolutionary Change in Proteins". Atlas of protein sequence and structure (volume 5, supplement 3 ed.). Nat. Biomed. Res. Found. pp. 345–358. ISBN 978-0-912466-07-1.
- Wing-Kin Sung (2010). Algorithms in Bioinformatics: A Practical Introduction. CRC Press. pp. 51–52. ISBN 978-1-4200-7033-0.
- Capriotti, Emidio, Remo Calabrese, and Rita Casadio. "Predicting the insurgence of human genetic diseases associated to single point protein mutations with support vector machines and evolutionary information." Bioinformatics 22.22 (2006): 2729-2734.
- Tümer, Z., et al. "Identification of point mutations in 41 unrelated patients affected with Menkes disease." American journal of human genetics 60.1 (1997): 63.
- Liu, Yujing, et al. "Mice with type 2 and 3 Gaucher disease point mutations generated by a single insertion mutagenesis procedure (SIMP)." Proceedings of the National Academy of Sciences 95.5 (1998): 2503-2508.
- Li, Dean Y., et al. "Elastin point mutations cause an obstructive vascular disease, supravalvular aortic stenosis." Human molecular genetics 6.7 (1997): 1021-1028.
- Zou, Jizhong, et al. "Site-specific gene correction of a point mutation in human iPS cells derived from an adult patient with sickle cell disease." Blood, The Journal of the American Society of Hematology 118.17 (2011): 4599-4608.