سدیم نیترید
سدیم نیترید (Na 3 N) یک ترکیب معدنی است که برخلاف لیتیم نیترید و برخی دیگر از نیتریدها، یک نیترید فلز قلیایی بسیار ناپایدار است. با ترکیب پرتوهای اتمی سدیم و نیتروژن که بر روی یک لایه یاقوت کبود دمای پایین رسوب میکنند، میتوان آن را ایجاد کرد.[1] این ماده به راحتی به عناصر خود تجزیه میشود:
- 2 Na 3 N → 6 Na + N 2
| سدیم نیترید | |
|---|---|
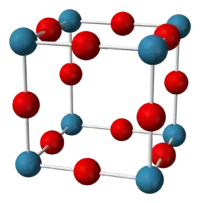 | |
Sodium nitride | |
| شناساگرها | |
| شماره ثبت سیایاس | ۱۲۱۳۶-۸۳-۳ |
| |
| خصوصیات | |
| فرمول مولکولی | Na3N |
| ترکیبات مرتبط | |
| دیگر آنیونها | Sodium imide سدیم آمید |
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |
| | |
| Infobox references | |
|
| |
تشکیل
سدیم نیترید را میتوان به دو روش مختلف تولید (سنتز) کرد:با تجزیه حرارتی از NaNH 2 یا با واکنش مستقیم از عناصر.[2] رایجترین روش برای تولید موفقیتآمیز سدیم نیترید توسط دیتر فیشر(به انگلیسی: Dieter Fischer)، مارتین جانسن (به انگلیسی: Martin Jansen) و گریگوری واجنین (به انگلیسی: Grigori Vajenine) با استفاده از روش دومی انجام شدهاست. راه اول تعیین نسبت مورد نظر از Na و N 2 در فاز گاز به صورت جداگانه و وارد کردن آنها در یک محفظه خلاء در بستر سرد میباشد، که سپس تا دمای اتاق (298 K) گرم میشود تا تبلور شود.[1] روش دوم واکنش سدیم اولیه با نیتروژن فعال شده با پلاسما بر روی یک سطح فلز است. با وارد کردن آلیاژ Na-K مایع به ترکیب و با حذف مایع اضافی و شستشو با آلیاژ تازه، میتوان این سنتز را بیشتر تسهیل کرد. سپس ماده جامد با استفاده از سانتریفیوژ از مایع جدا میشود. با این حال روش واجنین بسیار حساس به هوا است و میتواند به سرعت تجزیه شده و بسوزد، مگر اینکه در محیط اکسیژن خالص (O 2) قرار گیرد.[3]
ویژگیها
سدیم نیترید میتواند از رنگ قهوه ای مایل به قرمز یا آبی تیره بسته به تولید ترکیب به دلیل خواص ذاتی باشد.[1][3] بعد از چند هفته در دمای اتاق، هیچ نشانه ای از تجزیه نشان نمیدهد.[3] این ترکیب نقطه ذوب ندارد؛ زیرا همانطور که با استفاده از طیفسنجی جرمی در حدود ۳۶۰ کلوین ثابت شدهاست، دوباره به فرمهای اولیه آن تجزیه میشود.[1][2] تخمین آنتالپی تشکیل برای این ترکیب، ۶۴ کیلوژول بر مول است.[3]
کاربردها
این ماده در کارخانجات در رنج وسیعی از رنگهای و رنگدانهها، در صنعت داروسازی به عنوان یک حد واسط در تولید ساخارین و کافئین، در واکنشهای آلی تولید حشره کش و علف کشها به عنوان مهار کنندهٔ خوردگی، در صنعت نساجی به عنوان یک عامل سفید کننده، در صنعت لاستیک به عنوان بازدارندهٔ پلیمری، در برنامههای کاربردی شامل تصفیه آب، مایعات ضد انجماد، کیسه هوای خودروها، پاک کنندههای صنعتی و روانکنندهها کاربرد دارد. در صنایع مختلف از جمله صنایع خودروسازی و حمل و نقل هوایی، نیتریت سدیم برای درمان گرما و حرارت شیمیایی فلزات، آلیاژها و بخشی از آنها استفاده میشود. با توجه به خواص ضد خوردگی، نیتریت سدیم نیز به عنوان یک خنککننده در ذخیره انرژی حرارتی برای سیستمهای تهویه مطبوع و سردخانه صنعتی استفاده میشود.[4]
منابع
مشارکتکنندگان ویکیپدیا. «Sodium nitride». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۲ ژانویه ۲۰۲۱.
- Fischer, D. , Jansen, M. (2002). "Synthesis and structure of Na3N". Angew Chem. 41 (10): 1755. doi:10.1002/1521-3773(20020517)41:10<1755::AID-ANIE1755>3.0.CO;2-C. Fischer, D.; Cancarevic, Z.; Schön, J. C.; Jansen, M. Z. (2004). "Synthesis and structure of K3N". Z. Anorg. Allg. Chem. 630 (1): 156. doi:10.1002/zaac.200300280.. 'Elusive Binary Compound Prepared' Chemical & Engineering News 80 No. 20 (20 May 2002)
- Sangster, J. (2004). "N-Na(Nitrogen-Sodium) System". Journal of Phase Equilibria and Diffusion. 25 (6): 560–563. doi:10.1007/s11669-004-0082-0.
- Vajenine, G.V. (2007). "Plasma-Assisted Synthesis and Properties of Na3N". Inorganic Chemistry. 46 (13): 5146–5148. doi:10.1021/ic700406q. PMID 17530752.
- «نیترید سدیم - پتروکیمیاگر راد». www.pkrad.com. دریافتشده در ۲۰۲۱-۰۱-۱۲.