بیماری کبد چرب غیر الکلی
بیماری کبد چرب غیر الکلی (به انگلیسی: Non-alcoholic fatty liver disease) (به اختصار NAFLD) نوعی از کبد چرب است که در نتیجه تجمع چربی به دلیلی غیر از مصرف زیاد الکل در کبد بروز میکند. التهاب کبدی غیر الکلی (NASH) شدیدترین و پیشروندهترین نوع از NAFLD است و NAFLD شایعترین بیماری کبدی در کشورهای پیشرفته محسوب میشود.
| بیماری کبد چرب غیرالکلی | |
|---|---|
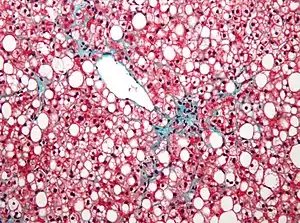 | |
| میکروگرافی از کبد چرب غیر الکلی، تغییر چرب مشخص شدهاست. لکههای سفیدرنگ مربوط به کبد چرب است. | |
| تخصص | پزشکی گوارش |
NAFLD با مقاومت به انسولین و سندروم متابولیک رابطه تنگاتنگی داشته و از سال ۲۰۱۷ ترکیب رژیم غذایی بهبود یافته و ورزش کارامدترین روش برای مدیریت NAFLD و کاهش مقاومت به انسولین بهشمار میروند. این بیماری ممکن است به درمانهایی که برای سایر حالات مقاومت به انسولین (مثل دیابت نوع دو) مثل متفورمین و تیازولیندیونها به وجود آمدهاند پاسخ دهد. حدود ۸۰ درصد از افراد چاق به این بیماری مبتلا هستند و ۲۰ درصد افراد در محدوده وزن عادی نیز ممکن است به آن مبتلا شوند. تخمین زده میشود ۲۴ درصد جمعیت جهان در سال ۲۰۱۷ تحت تأثیر این بیماری باشند. اگرچه در سال ۲۰۰۰ این بیماری به میزان زیادی ناشناخته بود، NASH و NAFLD دلایل اصلی بیماری مزمن کبدی در سال ۲۰۱۷ محسوب خواهند شد. حدود ۱۲ تا ۲۵ درصد افراد در ایالات متحده مبتلا به NAFLD و بین ۲ تا ۱۲ درصد افراد مبتلا به NASH هستند. بار اقتصادی آن در سالانه حدود ۱۰۳ میلیارد دلار آمریکا برآورد شدهاست (سال ۲۰۱۶). به نظر میرسد شیوع NAFLD/NASH به اندازه ای زیاد شود که به عامل اصلی پیوند کبد در سال ۲۰۲۰ تبدیل شود. دستورهای رسمی از سال ۲۰۱۶ توسط مرکز مطالعات بیماریهای کبدی آمریکا (AASLD)، مرکز مطالعات سلامتی و مراقبتی کشور پادشاهی انگلستان (NICE) و مرکز مطالعات کبد اروپا (EASL) فراهم شدهاست.
علائم و نشانهها
افراد مبتلا به NAFLD معمولاً بدون علامت هستند (یا علامت بارزی ندارند). NAFLD معمولاً با تستهای عملکرد کبدی طی آزمایش خون یا مشاهده تجمع چربی پس از نمونه برداری کبدی تشخیص داده میشود. در واقع، در صورت بروز علایم و نشانههای غیرطبیعی که به بیماری کبدی منتسب میشوند یا طی آزمایش خون بیماری NAFLD باید مورد بررسی قرار بگیرد. اگر نتایج آزمایشها عادی بوده و گزارشی بر بیماری کبدی دلالت نکند ولی تجمع چربی مشاهده شود سایر فاکتورهای خطرزا مثل چاقی، دیابت قندی، اختلال در ذخیره چربی یا دلایل دیگر مثل مصرف الکل باید مورد بررسی قرار بگیرند. بیماران ممکن است از خستگی، بیقراری و احساس ناراحتی بخاطر گرفتگی قسمت راست بالای حفره شکمی شکایت کنند. زردی متوسط، اگرچه به ندرت، نیز ممکن است دیده شود. مرکز مطالعات بیماریهای کبدی آمریکا (AASLD) بیماری NAFLD را به صورت زیر تعریف میکند: تجمع چربی در صورت نبود عامل دیگری که علت آن را در کبد توضیح دهد مثل الکل(۲۱ گرم الکل در هفته برای مردان و ۱۴ گرم الکل در هفته برای زنان)، تجمع چربی در صورت مصرف دارو، ارثی یا نقص تغذیه ای مادرزادی مثل کولین. NICE و EASL مصرف بیش از حد الکل (بیشتر از ۳۰ گرم در هفته برای مردان و ۲۰ گرم برای زنان)، تجمع چربی در اثر مصرف دارو، هپاتیت C و مشکلات سیستم غدد درون ریز را عوامل دیگر به وجود آورنده بیماریهای کبدی غیر مرتبط با NAFLD اعلام کردهاند.
عوامل خطرساز
هم آیندی NAFLD با سندروم متابولیک و مقاومت به انسولین رابطه تنگاتنگی دارد (چاقی، افزایش لیپید ترکیبی، دیابت قندی نوع ۲ و فشار خون بالا). علاوه بر مقاومت به انسولین، افزایش مداوم ترانس آمینازها، افزایش سن و BMI، عدم وجود یا میزان کم تولید هورمونهای هیپوفیز قدامی و کمبود اکسیژن در بافتهای بدن تحت نقص تنفسی طی خواب جزو عوامل زمینهساز بروز این بیماری محسوب میشوند. افراد غیر چاق مبتلا، بهطور مشخص، معمولاً نقص در حساسیت به انسولین داشته، کم تحرکند و خطر بالای بیماری قلبی و سطوح بالای لیپیدهای کبدی را دارند که معمولاً در نتیجه کاهش توانایی دستهبندی انواع چربی و عملکرد میتوکندریاییی در بافت چربی و افزایش تولید از نو (de novo) لیپید در کبد به وجود میآید. NAFLD در مردان تقریباً دو برابر زنان گزارش شدهاست (نتایج کاملاً تأیید شده نیست).
ژنتیک عوامل خطرساز ژنتیکی NAFLD نیز شناخته شدهاند. خانوادههایی با سابقه دیابت نوع دو ۶۶٫۶۷ درصد معمولاً بیش از یک فرد مبتلا به NAFLD دارند. علاوه بر این، افراد نژاد هیسپانیک (اسپانیایی و آمریکای لاتین) میزان شیوع بالاتری را نسبت به افراد سفیدپوست نشان دادهاند در حالیکه افراد سیاهپوست کمترین استعداد را در بروز این بیماری دارند. دو تغییر ژنتیکی در استعداد بروز این بیماری شناخته شده و در گروه بزرگی با پلی مورفیسم تک نوکلئوتیدی (SNP) غیر مترادف تأیید شدهاند ( PNPLA3 و TM6SF2 ). اگرچه NAFLD دلایل ژنتیکی هم دارد، انجمن AASLD غربالگری خانوادگی برای افراد خانواده فرد مبتلا پیشنهاد نمیکند چون هنوز مدارک کافی جهت تأیید ارثی بودن این بیماری وجود ندارد. مواردی از وقوع خانوادگی آن در مطاعات دوقلوها مشاهده شدهاست. ناهماهنگی زیستی در زمینه ناهماهنگی زیستی در محیط میکروبی روده و بیماریهای کبدی، بخصوص NAFLD، ارتباطات مستندی وجود دارد. بیماران NASH سطوح افزایش یافته اتانول در خون دارند. افراد با درجه شدیدتری از NAFLD نقص کولین مربوط به افزایش سوخت و ساز کولین را نشان دادهاند.
پاتوفیزیولوژی
براساس اعلام سازمان EASL، بیماری NAFLD میتواند تنها تجمع چربی، تجمع چربی با التهاب در لولهها و ورودی رگها بدون بالنی شدن ذرات چربی، یا تجمع چربی به همراه بالنی شدن ولی بدون التهاب را شامل شود. با بروز NASH، برخی ویژگیهای بافت شناختی مثل التهاب ورودی رگی، نفوذ هستههای چند گونه، اجسام مالوری و اجسام آپاپتوزی، هستههای حفره ای شفاف، تجمع چربی در رگهای بزرگ، میتوکندری عظیم و ظهور بافت فیبروزی در کنارههای رگی نیز ظهور مییابند که لزوماً نشانههای تشخیصی نیستند. مکانیزم مورد بحث دیگر نظریه «ضربه دوم» یا «آسیب بعدی» را مطرح میکند که بر اساس آن تجمع چربی کبدی تغییرات لازم را برای بروز التهاب کبدی ایجاد میکند. استرس اکسیداتیو، عدم تعادل هورمونی و وضعیت غیرعادی میتوکندریایی دلایل بالقوه پدیده «ضربه دوم» هستند. مدل تغذیه/ژنتیکی مدل «چند ضربه ای» را نیز ارائه میدهد که مدل ضربه دوم را با نشانههای زیستی بیماریهای دیگر و فاکتورهایی نظیر ژن و تغذیه ترکیب کرده و نتیجه را جهت پیشبینی تأثیر تغییرات شیوه زندگی و ژنتیکی برای تکامل پاتولوژی NAFLD به کار میبرد. NAFLD و بیماری کبد چرب الکلی از لحاظ ویژگیهای بافت شناختی مشابه بوده و بنابراین شاید بتوان گفت مسیرهای پاتوژنیک مشابهی دارند. در واقع، بیماران مبتلا به NASH سطوح افزایش یافته اتانول و پروتئوباکتری (که الکل تولید میکند) را در خونشان دارند و این ناهماهنگی زیستی به عنوان مکانیزمی برای این افزایش مطرح شدهاست.
تشخیص
نمونه برداری کبدی (آزمایش بافتی) تنها آزمایشی است که به صورت گسترده مورد قبول است (استاندارد طلایی) و NAFLD را از سایر انواع بیماری کبدی مشخص میکند (NAFLD و NASH)و میتواند شدت التهاب و فیبری شدن متعاقب آن را بسنجد. البته از آنجایی که اکثریت افراد مبتلا به NAFLD فاقد نشانه هستند، نمونه برداری از کبد جهت تشخیص کمی خطرناک به نظر میآید، فلذا روشهای دیگر مثل اولتراسونوگرافی ممکن است ارجحیت داشته باشند. برای کودکان و افراد جوانتر اولتراسونوگرافی پیشنهاد میشود اما همچنان نمونه برداری بهترین مدرک برای اثبات بروز بیماری است. آزمایشها عمومی خون برای بررسی عملکرد کبد به اندازه کافی برای تشخیص NAFLD حساسیت ندارند و نمونه برداری تنها روش قابل اتکایی است که با آن میتوان NAFLD را از NASH تمیز داد. افزایش آنزیمهای کبدی و عکسبرداری مافوق صوت نشان دهنده تجمع چربی از یافتههای مشترک در افراد مبتلا است. بر اساس دستورالعمل مؤسسه NICE، اندازهگیری سطوح آنزیم برای تشخیص NAFLD ناکارآمد بوده چون اغلب حتی در مراحل پیشرفته بیماری نیز در محدوده نرمال است. مؤسسه EASL غربالگری را فقط وقتی که مورد مشکوک به NAFLD است مجاز میداند و آن را نشانه کلیدی بروز احتمالی تکامل بیماری و بروز دیابت نوع دو، اتفاقات قلبی عروقی و افزایش فشار خون میداند. آزمایش خون برای تأیید تشخیص یا تعیین نرخ رسوب گلبولهای قرمز، گلوکز، آلبومین یا عملکرد کلیه مورد استفاده قرار میگیرد. کبد در تولید پروتئینهای تشکیل لخته خون نقش اساسی دارد و مطالعات مربوط به آن در قریب به اتفاق موارد در شرایط INR (نسبت بینالمللی نرمال شده) انجام میشوند. در افراد مبتلا به کبد چرب با آسیب التهابی آزمایش خون برای تعیین هپاتیتهای ویروسی (هپاتیت A, B,C و ویروسهای خانواده هرپس مثل اپشتاین بار یا سایتومگالوویروس)، روبلا و بیماریهای خودایمنی مورد استفاده قرار میگیرد. عملکرد پایین تیروئیدی در بیماران NASH شایع تر بوده که توسط هورمون محرک تیروئید تشخیص داده میشود. برخی آزمایشهای خون براساس نشانههای زیستی نیز از سال ۲۰۱۱ مورد استفاده قرار میگیرند اما مقبولیت عام ندارند. براساس دستورالعمل مؤسسه AASLD نمونه برداری کبدی در بیماران مبتلا به NAFLD که خطر ابتلا به التهاب کبدی یا فیبری شدن بافت کبد را دارند تنها در صورتی باید لحاظ شود که سایر عوامل مزمن بیماریهای کبدی مثل بیماریهای کبدی الکلی نفی شده باشند. بروز سندروم متابولیک، فیبری شدن بافت کبدی در NADFLD یا سفت شدن بافت کبدی (با MRE یا VCTE اندازهگیری میشود) نیز ممکن است برای تشخیص افراد با خطر بالاتر بروز التهاب کبدی یا فیبری شدن بافت کبدی مورد استفاده قرار بگیرند. همچنین، بیماران NAFLD باید تحت بررسی برای سرطان کبد و واریس مری قرار بگیرند. این مؤسسه معتقد است که یک گزارش مفید پاتولوژی باید بین NAFLD و NAFLD با التهاب کبدی و NASH (تجمع چربی با التهاب ورودی رگی و لوله ای و بالنی شدن سلولهای کبدی) در حضور یا عدم حضور بافت فیبری برای تشخیص شدت بیماری تفاوت قائل شود.
شناسایی
براساس دستورالعمل مؤسسه NICE آزمایش خون بهبود یافته فیبروز (ELF) دوره ای مداوم برای بررسی وقوع فیبری شدن پیشرفته هر سه سال برای بزرگسالان و هر دو سال برای کودکان ضروری است. پیگیری دوره ای نیز برای افراد چاق و مقاوم به انسولین با استفاده از مدل سوخت و سازی سنجش مقاومت به انسولین (HOMA-IR) پیشنهاد میشود. افراد مبتلا بهNASH و فیبری شدن بافت کبدی و فشار خون بالا نیز به دلیل خطر بالای پیشرفت بیماری باید تحت بازبینی مداوم قرار بگیرند.
نحوه مدیریت بیماری
دستورالعملهایی از سازمان مطالعه بیماریهای کبدی آمریکا (AASLD)، انستیتوی ملی صحت سلامتی و نگهداری (NICE)و سازمان اروپایی مطالعات کبدی (EASL) در این باره منتشر شدهاست. روش زندگی ترکیبی از تغذیه بهبود یافته و ورزش کارآمدترین راه برای مدیریت NAFLD و کاهش مقاومت به انسولین گزارش شدهاست. حمایتهای تشویقی مانند درمان رفتاری-شناختی نیز مؤثر بوده زیرا اکثریت افراد NAFLD را به عنوان بیماری درک نمیکنند و از این رو تمایل کمی جهت تغییر بروز میدهند. رژیم درمانNAFLD معمولاً بهبود تغذیه را نیز در برمیگیرد. افراد مبتلا به NAFLD ممکن است از رژیمهای غذایی با کربوهیدرات متوسط و پایین و چربی پایین بهرهمند شوند. رژیم غذایی مدیترانه ای نیز تأثیرات مطلوبی را طی برنامه ۶ هفته ای در کاهش التهاب و فیبری شدن القا شده توسط NASH به صورت مستقل از کاهش وزن نشان دادهاست. مؤسسه EASL محدودیت انرژی را به میزان کاهش ۵۰۰–۱۰۰۰ کیلوکالری در هفته نسبت به رژیم روزانه مؤثر میداند که باعث کاهش ۷ تا ۱۰ درصدی NAFLD به دلیل چاقی/افزایش وزن میشود. این کاهش با چربی کم تا متوسط نسبت به کربوهیدرات بالا یا کربوهیدرات کتوژنیک پایین و پروتئین بالا مثل رژیم مدیترانه ای و پرهیز از مصرف تمام غذاها و نوشیدنیهای حاوی فروکتوز را شامل میشود. دستورالعملهای انستیتو NICE مصرف ویتامین E را توصیه میکند اگرچه برای تمام مبتلایان به NAFLD مفید نیست. NICE مصرف مکمل اسید چرب امگا۳ را نیز به دلیل عدم وجود نتیجه قطعی در آزمایشها ابتدایی تصادفی پیشنهاد نمیکند. با اینحال برخی تحقیقات مروری سیستماتیک اذعان داشتهاند که مکملهای اسید چرب امگا۳ در افراد مبتلا NASH/NAFLD که میزان مصرفی حدود ۱ گرم در روز (میانه دوز ۴ گرم و طول دوره ۶ ماه) داشتند بهبود در چربی کبد را نشان دادند. بر اساس دستورالعمل AASLD، اسید چرب امگا۳ نباید به عنوان درمان NASH/NAFLD استفاده شود اما برای درمان افزایش تریگلیسیرید در بیماران مبتلا به NAFLD مجاز است. الکل نیز عامل وخیمکننده ای محسوب شده و در افراد NAFLD یا NASH باید مورد پرهیز قرار گیرد.EASL مصرف الکل زیر ۳۰ گرم در روز برای مردان و ۲۰ گرم در روز را برای زنان مجاز دانسته و محدودیتی از لحاظ مصرف قهوه لحاظ نمیکند. ترکیبات گیاهی علفی مانند خار مریم (Silymarin)، زردچوبه یا چای سبز در افزایش نشانگرهای زیستی و کاهش درجه NAFLD مؤثر دانسته شدهاند. .[۲۹]
دارو
درمان دارویی باید در موارد پیشرونده بیماری لحاظ شده و فقط برای افرادی که بیماری و بروز فیبروز کبدی توسط نمونه برداری در آنها به اثبات رسیده تجویز شود. اگرچه داروهای پایین آورنده قند خون برای کمک به کاهش چربی کبد مفید هستند، تا پایان سال ۲۰۱۵ هیچ داروی بخصوصی برای NASH یا NAFLD تأیید نشد. با آنکه به نظر میرسد که بسیاری از درمانها نشانگرهای بیوشیمیایی مثل سطوح آلانین ترانس آمینار را بهبود میبخشند بیشتر آنها تأثیر مشخصی روی معکوس کردن روند ناهنجاریهای بیوشیمیایی یا کاهش آسیبهای بافتی ندارند. حساس کنندگان به انسولین (متفومین و تیازولیدینها مثل پیگلیتازون) معمولاً برای کاهش مقاومت به انسولین در بیماران NAFLD استفاده میشوند و چندین تحقیق نشان دادهاند که تمام ویژگیهای بافتی NASH نشانگر التهاب کبدی و فیبری شدن بافت کبدی را بهبود میبخشد. با این وجود اثرات جانبی این داروها مثل پوکی استخوان، افزایش احتمال شکستگی استخوان، جمع شدن مایعات، نقص عملکردی احتقانی قلب، سرطان مثانه و افزایش وزن در دورههای مصرف بلند مدت استفاده از آنها را محدود کردهاست. به خاطر این اثرات جانبی، AASLD استفاده از پیگلتازون را فقط در بیمارانی که بیماری آنها توسط بیوپسی ثابت شدهاست مجاز میداند. AASLD مصرف متفورمین را به دلیل عدم نتیجه قطعی تحقیقات گذشته در مورد تأثیر آن بر حالت بافت کبدی، با توجه به بهبود مقاومت به انسولین و آمینوترانسفراز سرم، پیشنهاد نمیکند. NICE دستورالعمل مشابهی را در مورد پیگلتازون و مصرف آن به عنوان محافظت ثانویه بزرگسالان در برابر فیبروز کبدی پیشرفته، بدون توجه به وقوع دیابت، پیشنهاد میکند. مصرف ویتامین E نیز در بیمارانی که NASH در آنها توسط نمونه برداری به اثبات رسیدهاست مفید گزارش شدهاست. همچنین بهبود در بافت و بیوشیمی کبد در بیماران NAFLD که با استاتین مورد درمان قرار میگیرند نیز گزارش شدهاست. بیماران NAFLD درصد وقوع بالاتری از بیماری قلبی عروقی را دارند و از این نظر درمان با استاتین مؤثر به نظر میرسد. بنا بر گزارشها AASLD و EASL مبتلایان به NAFLD خطر ابتلای بیشتری به آسیبهای کبدی نسبت به افراد عادی ندارند. با این وجود، حتی اگر بتوان از استاتین در بیماران سیروز NASH استفاده نمود، در موارد NASH (نقص جبران نشونده) از مصرف آن باید اجتناب نمود. علاوه براین، استاتین در درمان نقص متابولیسم لیپیدی (dyslipidemia)در بیماران NAFLD پیشنهاد میشود. بنا بر دستورالعمل مؤسسه NICE، استفاده از استاتین در صوت عدم مشاهده دو برابر شدن آنزیمهای کبدی طی سه ماه پس از شروع مصرف دارو بلامانع است. درمان با پنتوکسی فیلین نیز بهبود ظاهر بافتی بافت چربی کبد را در شرایط میکروسکوپی در آزمایشهایی چند سبب شدهاست. آبتیکولیک اسید (Obeticholic acid) و الافیبرانور (Elafibranor)هنوز تحت آزمایش بوده و در لیست داروهای پیشنهادی AASLD در سال ۲۰۱۸ قرار ندارند. سین بیوتیک (ترکیب درمان پروبیوتیک و پری بیوتیک) نیز اثرات مطلوبی روی التهاب و عدم تعادل میکروارگانیسمهای دستگاه گوارش در بیمارانNAFLD داشتهاست.
جراحی
جراحی کوچک کردن معده (bariatric surgery) روش مؤثری برای افراد چاق و دیابتی مبتلا به NAFLD است که کاهش وزن و رفع التهاب NASH مثل فیبروز را در پی دارد. مؤسسه AASLD جراحی کوچک کردن معده را تنها در مورد NASH و به صورت موردی بر اساس برنامه آزمایشی جراحی معده مجاز میداند. مؤسسه EASL پیوند کبد را برای بیماران NASH در مراحل انتهایی بیماری کبد، از کارافتادگی کبد یا سرطان کبد روش پذیرفته شدهای دانسته و میزان بقا را قابل مقایسه با پیوند بافت در سایر بیماریها میداند. افراد NASH مبتلا به سروز در صورت لحاظ شدن برای پیوند باید به صورت مرتب برای بیماریهای قلبی عروقی مورد آزمایش قرار گیرند (حتی در صرت عدم وجود نشانههای مشخص). حدود ۹۲ درصد افراد مبتلا به NAFLD بهبود در التهاب کبدی و حدود ۷۰ درصد افراد بهبود تقریباً کاملی را پس از جراحی کوچک کردن معده مشاهده میکنند. به نظر میرسد NASH/NAFLD عامل اصلی پیوند کبد در سال ۲۰۲۰ باشد.
نتایج
دلیل اصلی این بیماری و مکانیسمهای پیشرفت بیماری از یک مرحله به مرحله بعد کاملاً مشخص نیستند، اگرچه یافتههای اخیر دیدگاههایی را در مورد مکانیسم آن فراهم کردهاند. NAFLD یک بیماری چند-سیستمی است که از عواملی چند (اندامها و مسیرها) به غیر از کبد تأثیر میپذیرد و بر آنها تأثیر میگذارد. نرخ پیشرفت فیبروز کبدی در انسانهای مبتلا به NASH تا ۷ سال تخمین زده میشود در حالیکه این میزان در NAFLD حدود ۱۴ سال است و این افزایش متناسب با مراحلی است که طی میشود و بر اساس ظواهر بالینی بیماری بین افراد متفاوت به اشکال مختلفی بروز میکند. فیبری شدن بافت کبد در NASH بسیار سریعتر از NAFLD بروز میکند. یک تحقیق بینالمللی نشان دادهاست که بیماران NAFLD در بازه ۱۰ ساله حدود ۸۱٫۵ درصد امکان بقای بیشتری دارند. NAFLD عامل خطرسازی در بروز فیبروز کبدی، افزایش فشار خون، بیماری حاد کلیوی، فیبریلاسیون قلبی، نقص میوکارد قلبی، سکته اسیکمیک و مرگ به دلایل قلبی عروقی (مدارک خیلی کم تا کم در مطالعات مشاهده ای) به شما رمیرود. NAFLD و NASH سبب افزایش خطر سرطان کبد میشوند. سروز و سرطان کبد ناشی از NAFLD دومین دلیل پیوند کبد در سال ۲۰۱۷ در آمریکا بود. ۴۵ درصد موارد NASH در غیاب سروز کبدی به سرطان کبد منجر میشود و افراد سروزی مبتلا به NASH خطر بالایی نسبت به احتمال بروز سرطان کبد دارند. در واقع، میزان بروز سرطان کبد در تقابل با NASH از سال ۲۰۰۲ تا سال ۲۰۱۲ در آمریکا افزایش ۴ برابری داشتهاست که بیشتر از هر عامل دیکر در بروز سرطان کبد محسوب میشود. NAFLD سومین عامل خطرساز در بروز سرطان کبد بهشمار میرود. NAFLD و NASH مشخصا به میزان ۲ تا ۳ درصد در NAFLD و ۱۵ تا ۲۰ درصد در NASH طی بازه زمانی ۱۰ تا ۲۰ ساله بروز مییابند. NAFLD همچنین میتواند زمینهساز بروز سندروم متابولیک باشد (اثرات دوسویه نفی نشدهاست). وجود و درجه فیبروز کبدی قویترین عامل تشخیصی در مرگ و میر ناشی از بیماری کبدی، بخصوص NAFLD بهشمار میرود. با آنکه NAFLD سبب سروز و سرطان کبد میشود، اکثریت مرگها در بیماران NAFLD ناشی از نقص قلبی عروقی است. مطالعه ۷ ساله ای در ۳۴۰۰۰ بیمار NAFLD نشان داده که ۶۵ درصد آنها خطر بروز حوادث قلبی، کشنده یا غیر کشنده، دارند.
رفتارشناسی
حدود ۹ تا ۳۶٫۹ درصد افراد در قسمتهای مختلف دنیا مبتلا به بیماری کبد چرب غیر الکلی هستند. تحقیقات بر اساس میزان افزایش یافته آنزیمهای کبدی سبب تخمین کمتر از حد شیوع جهانی آن شد و سونوگرافی با امواج فراصوت و اسپکتروسکوپی پروتون NMR بود که مشخص کرد حدود ۲۵ درصد جمعیت تحت تأثیر NAFLD و NASH هستند. قریب به ۲۰ درصد از جمعیت در ایالات متحده مبتلا به بیماری کبد چرب غیر الکلی هستند. شیوع تقریباً مشابهی از این بیماری در اروپا و کشورهای آسیا-اقیانوسیه وجود دارد (اطلاعات کمتری از آن در دست است). میزان شیوع در کودکان ۱ تا ۱۹ حدود ۸ درصد جمعیت کلی تا حدود ۳۴ درصد در افراد تحت رصد کلینیکهای چاقی کودکان تخمین زده شدهاست. نسبت به سالهای دهه ۲۰۰۰ در آمریکا شیوع NAFLD حدود ۲ برابر و شیوع NASH تقریباً ۲٫۵ برابر شدهاست. NASH و NAFLD میزان شیوع بیشتری در جمعیت آمریکای لاتین دارند، که احتمالاً به دلیل نرخ بالاتر چاقی و دیابت نوع دو در این جمعیت است. میزان وقوع این بیماری در سفید پوستان متوسط و در سیاه پوستان در کمترین حد است. این بیماری شایعترین بیماری کبدی مزمن در کودکان و جوانان و بزرگسالان است. مردان دو برابر بیش از زنان به NAFLD مبتلا میشوند. اگرچه اکثر موارد این بیماری در افراد چاق دیده میشود، سهم بزرگی از افراد مبتلا در محدوده وزنی عادی و حتی لاغر هستند. NAFLD بین ۱۰ تا ۲۰ درصد از آمریکایی و اروپاییهای لاغر را تحت تأثیر قرار میدهد (برخی کشورها از جمله هند، نرخ بیشتری در وقوع NAFLD در افراد لاغر داشته در صورتی که NAFLD در افراد چاق در آنها دیده نمیشود). با توجه به گروهی از مطالعات جهانی، NAFLD در افراد لاغر نیز خطرات مشابه افراد چاق را در پی دارد (با میانه پایینتر از میزان درمان به غیر از موارد پیوند کبد). PNPLA3 ممکن است عامل مؤثری در پیشرفت NAFLD در افراد لاغر بهشمار رود. با توجه به مطالب گفته شده، افراد مبتلا به NAFLD باید فارغ از عامل چاقی تحت درمان قرار بگیرند.
تاریخچه
اولین مورد شناخته شده از بیماری کبد چرب غیر الکلی در سال ۱۹۵۲ توسط ساموئل زلمان شناخته شد. زلمان مطالعاتش را با مشاهده کبد چرب در یکی از پرسنل بیمارستان که هر روز بیش از ۲۰ قوطی کوکاکولا مینوشید شروع نمود. وی سپس با طراحی آزمایشی در ۲۰ فرد چاق غیر الکلی به مدت یک سال و نیم متوجه شد که تقریباً نیمی از این افراد به صورت مشخص کبد چرب دارند. کبد چرب حداقل از سال ۱۷۸۴ با دیابت، بیماری قلبی عروقی و تخلیه کولین و از سال ۱۹۴۹ با قند مربوط بودهاست. همچنین حداقل از ۱۹۳۰ عامل مشترکی با احتمال وقوع بالا در دیابتهای شدید محسوب میشدهاست. نام "التهاب کبدی غیر الکلی NASH" بعدتر در سال ۱۹۸۰ توسط یورگن لودویگ و همکارانش از کلینیک مائو برای بالا بردن آگاهی در مورد پاتولوژی وقوع این بیماری تعریف شد (چون برخی گزارشهای پیشین به دلیل دروغ گفتن بیماران نادیده گرفته میشد). این مقاله در زمان خودش نادیده گرفته شد اما در میانه ۱۹۹۰ که این حالت تحت مطالعه قرار گرفت و دیدارهای بینالمللی در مورد این موضوع به سال ۱۹۹۸ برپا شد به عنوان مقاله ای شاخص به میدان آمد. واژه NAFLD با تعریف جامع تر از سال ۲۰۰۲ مورد استفاده قرار گرفت. ویژگیهای تشخیصی به کار برده شدند و در سال ۲۰۰۵ شبکه تحقیقاتی درمانی کمیته پاتولوژی سازمان جهانی بهداشت سیستم درجهبندی NAS را ابداع کرد.
کودکان
بیماری کبد چرب غیر الکلی در کودکان برای اولین بار در سال ۱۹۸۳ گزارش شد و تا سال ۲۰۰۷ معمولترین بیماری حاد کبد در میان کودکان و نوجوانان بود که حدود ۲۰ درصد از آنها را در آمریکا، تنها در سال ۲۰۱۶، مبتلا کرد. بیماری NAFLD با سندروم متابولیک که مجموعه ای از عوامل خطرساز بروز بیماری قلبی عروقی و دیابت نوع ۲ بهشمار میرود مربوط است. مطالعات نشان دادهاند که چاقی شکمی و مقاومت به انسولین، به خصوص، از عوارض اصلی آن بهشمار میروند. بیماریهای کبدی دیگر مثل هپاتیت سی یا بیماریهای قلبی عروقی نیز سبب افزایش خطر بروز NAFLD هستند. با آنکه سن تشخیص در کودکان بین ۱۱ تا ۱۳ سال است برخی کودکان در ۲ سالگی مورد تشخیص قرار گرفتهاند. میانگین سن تشخیص معمولاً ۱۰ سال بوده و با توجه به اینکه نشانههای غیر اختصاصی نیز در کودکان گزارش شدهاست تشخیص NAFLD در آنها سخت است. پسرها احتمال بروز بالاتری نسبت به دخترها دارند. اضافه وزن یا حتی افزایش وزن در کودکی و نوجوانی با افزایش خطر NAFLD در دوران بعدتر زندگی وجود دارد و در مطالعهٔ ادامهدار ۳۱ ساله BMI، سطوح انسولین پلاسما، مرد بودن، سابقه ژنتیکی (واریته ژنهای PNPLA3 و TM6SF2) و وزن کم هنگام تولد از عوامل خطرساز بروز NAFLD در بزرگسالی معرفی شدند. در مطالعه ای التهاب اولیه در ۴۵ درصد از کودکان مشکوک به بروز NAFLD مشاهده شد. پیشبینی بروز بیماری در کودکان با التهاب اولیه سختتر بوده و در مقایسه با بزرگسالان، تعداد بیشتری از NAFLD به NASH میرسند. در واقع، آمار ۱۷ تا ۲۵ درصدی از کودکان NAFLD که به NASH مبتلا میشوند و ۸۳ درصدی از کودکان مبتلا به چاقی شدید (این میزان در بزرگسالان ۲۹ درصد است) نشان میدهد که فیبروز کبدی در کودکان پیشرفت سریعتری نسبت به بزرگسالان دارد. تشخیص زودهنگام NAFLD در کودکان میتواند مانع پیشرفت بیماری کبدی طی بزرگسالی شود. با توجه به اینکه اغلب موارد NAFLD در کودکان فاقد علامت بوده و تنها حدود ۴۲ تا ۵۹ درصد با دردهای شکمی مراجعه میکنند این مسئله چالش بزرگی بهشمار میرود. نشانههای دیگر درد در یک چهارم راست بالایی شکم یا تغییر رنگ پوست در چینهای بدن (این نشانه اغلب در بیماران NASH دیده شدهاست) یا افزایش اندازه کبد (در ۳۰ تا ۴۰ درصد کودکان) میباشند. نمونه برداری کبد برای تشخیص در کودکان تنها در تشخیص غیر دقیق یا پیش از شروع درمان سمیت کبدی ASSLD مجاز میباشد. EASL پیشنهاد میکند که آزمایشهای فیبروز مانند الاستومتری، تصویربرداری از ضربهٔ نیروی تشعشع آکوستیک یا نشانههای زیستی سرم به منظور کاهش تعداد نمونه برداری مورد استفاده قرار گیرد. بر اساس پروتکل مؤسسه NICE کودکان هر دو سال یک مرتبه باید تحت آزمایش خون ELF به منظور سنجش منظم فیبروز کبدی پیشرفته قرار گیرند. چندین مطالعه نیز عکسبرداری مغناطیسی رزونانس الاستوگرافی را به عنوان جایگزینی برای سونوگرافیهای فراصوت که کمتر مورد اعتماد هستند پیشنهاد دادهاست. بنا بر AASLD و EASL، تغییرات شدید نحوه زندگی مانند فعالیت فیزیکی یا تغییرات رژیم غذایی نیز اولین گامهای درمانی بهشمار میروند که بافت کبد و سطوح انتقال دهندههای آمین را بهبود میبخشند. از دیدگاه درمان دارویی، استفاده از متفورمین در کودکان باید پرهیز شود ولی مصرف ویتامین E میتواند سبب افزایش سلامت کبدی شود. NICE مصرف ویتامین E را برای کودکان با فیبروز شدید کبدی، فارغ از اینکه مبتلا به دیابت باشند یا نه، توصیه میکند. تنها درمان کاملاً مؤثر در NAFLD کودکان کاهش وزن است. مدارکی در دست است که نشان میدهند فقر تغذیه یا تغذیه بیش از حد مادری نیز احتمال NASH کودکی و وقوع آن طی زندگی را تشدید میکند.
تشخیص و نشانگان زیستی
با توجه به مهاجم بودن نمونه برداری کبدی و سختی تخمین نرخ وقوع آن، روشهای تشخیص و کنترل ارزان و غیر تهاجمی در پیشرفت بیماری NAFLD جزو ضروریات تحقیق بهشمار میروند. جستجوی نشانگان زیستی NAFLD، میزان دخالت NAFLD و NASH در مطالعات بررسی چربیها، تصویربرداری پزشکی، مطالعات بررسی پروتئینها، آزمایشهای خونی و سیستمهای درجهبندی نیز در درجات بعدی اهمیت قرار داند. الاستوگرافی رزونانس مغناطیسی حساسیت خوبی برای سنجش چربی کبدی داشته و دقت بالایی در پیدا کردن فیبروز کبدی در NAFLD فارغ از BMI و التهاب نشان دادهاست و بنابراین جایگزین قابل اتکایی برای تشخیص NAFLD و بروز NASH در مقایسه با سونوگرافی فراصوت و آزمایش خون بهشمار میرود بر اساس مقالات مروری مجله Nature در سال ۲۰۱۸، تخمین چگالی پروتون چربی توسط الاستوگافی رزونانس مغناطیسی (MRI-PDFF) دقیقترین و صحیحترین و حتی استاندارد طلایی سنجش التهاب کبدی استئاتوزیس محسوب میشود. الاستوگرافی فراصوت (فیبرو اسکن) برای تشخیص فیبروز و سروز در تنظیمات روزانه پزشکی، با دقت بالاتر از سونوگرافی فراصوت و صحت کمتر از الاستوگرافی رزونانس مغناطیسی، و قطعات اسکلت سلولی پلاسمایی 18 (CK18) که نشانه زیستی تقریباً دقیقی از التهاب کبدی استئاتوزیس است برای تشخیص پیشنهاد میشود.
تولید دارو
تولید دارو برای NASH بسیار فعال و به سرعت در حال پیشرفت است. داروهای نو با هدف قرار دادن محلهای متنوع بین کبدی، از تنظیم تولید لیپید و هومئوستاز گلوکز، تا استرس اکسیداتیو و مراکز میتوکندریایی در سلولهای کبدی، سیگنالهای التهابی روی سلولهای کبدی و هدفهای بین سلولی مرتبط با فعالسازی سلولهای ستاره ای و فیبروژنز طراحی و تولید میشوند. تا ۲۰۱۸ آزمایشهای کلینیکی روی cenicriviroc, elafibranor, obeticholic acid و Selonsertib در مرحله ۳ و چندین مورد دیگر در مرحله دوم در جریان بودند. با توجه به اینکه NAFLD یک بیماری پیچیدهاست که چندین اندام و بافت را درگیر میکند، درمانهای ترکیبی (مواد ترکیبی) و درمانهای توأم (ترکیب داروها و درمانهای غر دارویی مانند درمانهای رفتاری یا تغییرات شیوه زندگی) نیز جهت بالا بردن کارایی داروها مؤثر به نظر میرسند. توجه به این نکته حائز اهمیت است که اکثریت دورههای آزمایشگاهی کوتاه و بین ۳ تا ۱۸ ماه هستند در حالیکه در دنیای واقعی استفاده از آنها طولانی مدت و مداوم خواهد بود.
لابی گری
در فرانسه، سندیکای نوشیدنیهای غیر الکلی (Boissons Rafraîchissantes de France) و تولیدکنندگان نوشابه مثل کوکاکولا فرانسه، Orangina و کارخانه پپسی فرانسه توسط مجله (Canard Enchainé) برای به کار بردن تیتر "فهم بهتر پاتولوژی NASH" در وبسایت که توضیح میدهد "پاتولوژی بیماری NASH که گاهی بیماری نوشابه نیز نامیده میشود سواستفاده زبانی بوده و چون ارتباط مستقیمی بین مصرف نوشیدنیهای غیرالکلی با آن وجود ندارد میانبر معنایی نادرستی به شمار میرود" تحت پیگرد قانونی قرار گرفتند. سایر صفحات وبسایت مانند تیتر "نه به اطلاعات غلط" نیز پس از آن حذف شدند.
منابع
- مشارکتکنندگان ویکیپدیا. «Non-alcoholic fatty liver disease». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۲۰ اکتبر ۲۰۱۸.