گاز ایدهآل
گاز آرمانی[1] یا گاز ایدهآل (به انگلیسی: Ideal gas)، گازی است که فقط در تئوری وجود دارد، و شامل تعداد زیادی ذرات نقطه ای متحرک است که تنها برهم کنش آنها برخودهای کاملاً الاستیک است. مفهوم گاز ایدهآل بسیار کاربردی است چرا که از قانون گاز ایدهآل پیروی میکند. قانون گاز ایدهآل یک معادله حالت ساده است و برای استفاده در مکانیک آماری مناسب است.[2]
| ترمودینامیک |
|---|
 |
|
در بسیاری از شرایط عادی، رفتار بسیاری از گازهای واقعی از نظر کیفی بسیار شبیه به گاز ایدهآل است. بسیاری از گازها از قبیل نیتروژن، اکسیژن، هیدروژن و گازهای نجیب و همچنین برخی گازهای سنگین تر از قبیل کربن دیاکسید را میتوان تا دقتهای بالایی گاز ایدهآل فرض کرد.[3] به صورت کلی گازها هر چه دمای بیشتر و فشار کمتری داشته باشند به گاز ایدهآل نزدیک تر خواهند بود.[3] در دماهای پایین و فشارهای بالا، نیروهای بین مولکولی و فاصلهها تاثیرگذارتر بوده و در نتیجه اگر گاز را گاز ایدهآل در نظر بگیریم خطای زیادی خواهیم داشت، مانند بسیاری از مبردها یا گازهایی که نیروهای بین مولکولی قوی دارند مانند، بخار آب.
قانون گازهای ایدهآل
گازهای ایدهآل در حالت تعادل داخلی از معادلهٔ گاز ایدهآل پیروی میکنند:
که در آن P فشار داخلی مجموعه، V حجم مجموعه، n تعداد مولهای ذرات مجموعه، R ثابت جهانی گازها و T دمای مجموعه با یکای کلوین است.
اثبات
برای اثبات این قانون، اول لازم است که با قانونهای بویل و شارل آشنا شویم.
قانون بویل
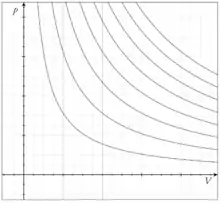
رابطهٔ بین فشار و حجم یک گاز در ۱۶۶۲ میلادی توسط رابرت بویل (Robert Boyle) اندازهگیری شد. بویل متوجه شد که افزایش فشار وارد شده بر یک گاز با کاهش حجم آن متناسب است. اگر فشار دو برابر شود، حجم به نصف کاهش مییابد. اگر فشار سه برابر شود، حجم به یک سوم حجم اولیه اش میرسد. قانون بویل میگوید که در دمای ثابت، حجم گاز با فشار رابطهٔ عکس دارد:
قانون شارل
رابطهٔ بین حجم و دمای یک گاز در ۱۷۸۷ میلادی توسط ژاک شارل (Jacques Charles) مطالعه شد و نتایج او بهطور قابل ملاحظهای توسط شاگردانش ژوزف گیلوساک (Joseph Gay - Lussac) گسترش یافت. براساس این قانون حجم تمام گازها، در فشار ثابت، با دمای مطلق آن گاز رابطهٔ مستقیم دارد:
قانون گازهای ایدهآل
در دما و فشار ثابت حجم یک گاز با تعداد مولهای آن نسبت مستقیم دارد. حجم یک مول گاز نصف حجم اشغال شده توسط ۲ مول گاز میباشد؛ بنابراین قانون و قوانین بویل و شارل میتوان گفت که:
با استفاده از یک عدد ثابت میتوان تناسب را به تساوی تبدیل کرد:
که از آن نتیجه میشود:
قانون گازهای ایدئال توسط نظریهٔ جنبشی گازها
نمونهای از یک گاز شامل N (عدد آووگادرو) مولکول، هر کدام با جرم m را در نظر بگیرید. اگر این نمونه در مکعبی با یال a باشد، حجم آن برابر خواهد شد با:
با فرض اینکه یک سوم مولکولها در جهت محور x، و دو سوم در جهت محورهای y و z حرکت کنند، آنگاه در هر ۲a حرکت یک مولکول گاز در جهت محور x داخل مکعب، مولکول حداقل یکبار به دیوارهٔ مکعب برخورد میکند. با فرض اینکه سرعت میانگین هر مولکول گاز برابر u است، در هر ثانیه هر مولکول گاز به اندازهٔ برخورد دارد و در هر برخورد به اندازهٔ ۲mu اندازهٔ حرکت آن تغییر میکند. پس در هر ثانیه هر مولکول گاز به اندازهٔ زیر به دیوارهٔ مکعب نیرو وارد میکند:
از این رو برای تمام مولکولهای گاز میتوان نوشت: S
فشار عبارت است از نیرو بر سطح. پس:
پس میتوان نوشت:
که KE در آن میانگین انرژی جنبشی مولکولی گاز میباشد؛ و از آنجا که انرژی جنبشی یک گاز (بنابر نظریه جنبشی گازها) با دمای مطلق آن نسبت مستقیم دارد و همچنین ، پس:
که با ضرب کردن عدد ثابتی مثل R، میتوان تناسب را به تساوی تبدیل کرد:
جستارهای وابسته
منابع
- «گاز آرمانی» [فیزیک] همارزِ «گاز ایدهآل» (به انگلیسی: ideal gas)؛ منبع: گروه واژهگزینی. جواد میرشکاری، ویراستار. (۱۳۷۶-۱۳۸۵). فرهنگ واژههای مصوب فرهنگستان. تهران: انتشارات فرهنگستان زبان و ادب فارسی. شابک ۹۷۸-۹۶۴-۷۵۳۱-۷۷-۱ (ذیل سرواژهٔ ideal gas1)
- "Ideal gas". Wikipedia. 2020-04-17.
- Cengel, Yunus A.; Boles, Michael A. Thermodynamics: An Engineering Approach (4th ed.). p. 89. ISBN 0-07-238332-1.