نیترید سیلیسیم
نیترید سیلیسیم یک ترکیب شیمیایی از عناصر سیلیکون و نیتروژن است .
| نیترید سیلیسیم | |
|---|---|
 Sintered silicon nitride ceramic | |
Preferred IUPAC name Silicon nitride | |
دیگر نامها Nierite | |
| شناساگرها | |
| شماره ثبت سیایاس | 12033-89-5 |
| پابکم | 3084099 |
| کماسپایدر | 2341213 |
| UNII | QHB8T06IDK |
| شمارهٔ ئیسی | 234-796-8 |
| MeSH | Silicon+nitride |
| جیمول-تصاویر سه بعدی | Image 1 |
SMILES
| |
| |
| خصوصیات | |
| فرمول مولکولی | N4Si3 |
| جرم مولی | ۱۴۰٫۲۸ g mol−1 |
| شکل ظاهری | grey odorless powder[1] |
| چگالی | 3.17 g/cm3[1] |
| دمای ذوب | ۱٬۹۰۰ درجه سلسیوس (۳٬۴۵۰ درجه فارنهایت؛ ۲٬۱۷۰ کلوین)[1] (decomposes) |
| انحلالپذیری در آب | Insoluble[1] |
| ضریب شکست (nD) | 2.016[2] |
| خطرات | |
| طبقهبندی ئییو | not listed |
| خطرات اصلی | When heated to decomposition, silicon nitride may emit toxic fumes of ammonia and ozone. Contact with acids may generate flammable hydrogen gas.[3] |
| ترکیبات مرتبط | |
| دیگر آنیونها | silicon carbide silicon dioxide |
| دیگر کاتیونها | boron nitride |
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |
| | |
| Infobox references | |
|
| |
Si
3N
4 از نظر ترمودینامیکی پایدارترین نیتریدهای سیلیسیم است. از این رو ، Si
3N
4 هنگام اشاره به اصطلاح "نیترید سیلیکون" از نظر تجاری مهمترین نیتریدهای سیلیکون است . این یک ماده جامد سفید با نقطه ذوب بالا است که نسبتاً شیمیایی بی اثر است و توسط HF رقیق و H
2SO
4 گرم مورد حمله قرار می گیرد. بسیار سخت است (8.5 در مقیاس mohs ). از پایداری حرارتی بالایی برخوردار است.
تولید
مواد با حرارت دادن سیلیکون پودر شده بین سال 1300 و 1400 درجه سانتیگراد در محیط ازت تهیه می شود و 1400 درجه سانتیگراد در محیط ازت:
وزن نمونه سیلیکون به دلیل ترکیب شیمیایی سیلیسیم و ازت به تدریج افزایش می یابد. بدون کاتالیزور آهن ، واکنش پس از چند ساعت کامل می شود ، در حالی که هیچ افزایش وزن بیشتری به دلیل جذب نیتروژن (در هر گرم سیلیسیم) مشاهده نمی شود. علاوه بر سیلیکون نیترید ، چندین مرحله دیگر نیترید سیلیکون (با فرمول های شیمیایی مربوط به درجات مختلف نیتریداسیون / حالت اکسیداسیون Si) در ادبیات گزارش شده است ، به عنوان مثال ، مونونیترید disilicon گاز ( Si
2N ) مونونیترید سیلیکون (SiN) ، و سسکوینیترید سیلیکون ( Si
2N
3 ) که هر کدام از مراحل فاز استوکیومتری هستند. همانند سایر مواد نسوز ، محصولات بدست آمده در این سنتزهای دمای بالا به شرایط واکنش (به عنوان مثال زمان ، دما و مواد اولیه از جمله واکنش دهنده ها و مواد ظرف) و همچنین نحوه تصفیه بستگی دارد. با این حال ، از آن زمان وجود سسکوینیترید زیر سوال رفته است. [4]
همچنین می توان آن را از طریق راه دییمید تهیه کرد: [5]
- در دمای صفر درجه سانتی گراد:
- در دمای 1000 درجه سانتی گراد:
کاهش کاربوترمال دی اکسید سیلیسیم در جو نیتروژن در 1400–1450 درجه سانتی گراد نیز مورد بررسی قرار گرفته است: [5]
نیتراسیون پودر سیلیسیم در دهه 1950 و به دنبال "کشف مجدد" نیترید سیلیکون ایجاد شد و اولین روش در مقیاس بزرگ برای تولید پودر بود. با این حال ، استفاده از سیلیکون خام با خلوص کم باعث آلودگی نیترید سیلیسیم توسط سیلیکات ها و آهن می شود . تجزیه دییمید منجر به نیترید سیلیکون آمورف می شود که نیاز به بازپخت بیشتر در زیر ازت در 1400-1500درجه سانتی گراد دارد برای تبدیل آن به پودر کریستالی ؛ این اکنون دومین مسیر مهم برای تولید تجاری است. کاهش کاربوترمال اولین روش مورد استفاده برای تولید نیترید سیلیکون بود و اکنون به عنوان مقرون به صرفه ترین مسیر صنعتی برای خلوص پودر نیترید سیلیکون در نظر گرفته شده است. [5]
فیلمهای نیترید سیلیکونی درجه الکترونی با استفاده از رسوب بخار شیمیایی (CVD) یا یکی از انواع آن مانند رسوب بخار شیمیایی تقویت شده با پلاسما (PECVD) تشکیل می شود: [5]
در دمای 750-850 درجه سانتیگراد
برای نشست لایه های نیترید سیلیکون روی لایه های نیمه رسانا (معمولاً سیلیکون) ، از دو روش استفاده می کنند:
- فناوری رسوب بخار شیمیایی با فشار کم (LPCVD) ، که در دمای نسبتاً بالا کار می کند و در لوله کوره افقی یا عمودی قرار گرفته است، [6] یا
- فناوری رسوب با افزایش پلاسما بخار شیمیایی (PECVD) ، که در شرایط کم دما و خلا کار می کند.
ثابت های شبکه ای نیترید سیلیکون و سیلیکون متفاوت است. بنابراین، تنش یا استرس می تواند بسته به فرآیند رسوب رخ دهد. به خصوص هنگام استفاده از فناوری PECVD این تنش میتواند با استفاده از پارامترهای تنظیم رسوب کاهش یابد. [7]
نانوسیم های نیترید سیلیکون را می توانند با استفاده از روش سل-ژل و با استفاده از احیا کربوترمال و به دنبال آن نیتراسیون ژل سیلیکا ، که حاوی ذرات کربن فوق العاده ریز است ، تولید شوند. ذرات را می توان با تجزیه دکستروز در محدوده دما 1200-1350 درجه سانتیگراد تولید کرد واکنشهای احتمالی سنتز عبارتند از: [8]
پردازش
تولید نیترید سیلیکون به عنوان یک ماده حجیم دشوار است - نمی توان آن را بیش از 1850 درجه سانتی گراد گرم کرد ، که بسیار پایین تر از نقطه ذوب آن می باشد، به دلیل جدا شدن سیلیکون از نیتروژن. بنابراین ، استفاده از تکنیک های متداول پرس ایزواستاتیک گرم مشکل ساز خواهد بود. اتصال پودرهای نیترید سیلیکون را می توان در دماهای پایین از طریق افزودن مواد اضافی (کمک ذوب یا "چسب") که معمولاً درجه ای از ذوب فاز مایع را القا می کند ، به دست آورد. [9] یک جایگزین بهتر استفاده از پخت پلاسما جرقه ای می باشد که در آن حرارت به سرعت با عبور پالس های جریان الکتریکی از پودر فشرده شده انتقال داده میشود. فشرده سازی نیترید سیلیسیم چگال توسط این تکنیک ها در دمای 1500-1700 سانتی گراد بدست آمده است.[10] [11]
ساختار کریستال و ویژگی هایش
| Blue atoms are nitrogen and grey are silicon atoms | ||||||
|---|---|---|---|---|---|---|
|
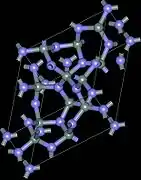
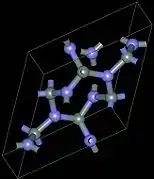
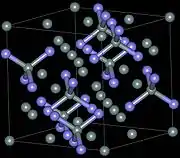
سه ساختار کریستالوگرافی نیترید سیلیکون وجود دارند که به عنوان فازهای α ، β و γ تعیین می شوند. [12] فازهای α و β رایج ترین اشکال سیلیکون نیترید هستند، و می تواند تحت شرایط فشار عادی تولید شوند. فاز γ فقط در فشار و درجه حرارت های بالا می تواند سنتز شود و دارای سختی 35GPa است. [13] [14]
سیلیکون نیترادهای آلفا و بتا به ترتیب دارای ساختارهای سه ضلعی ( نماد پیرسون hP28 ، گروه فضایی P31c ، شماره 159) و شش ضلعی (hP14 ، P6 3 ، شماره 173) هستند که با استفاده از SiN
4 چهاروجهی گوشه ای ساخته می شوند . آنها را می توان به ترتیب متشکل از لایه های اتم سیلیسیم و نیتروژن در توالی ABAB ... یا ABCDABCD ... در سیلیکون نیترید های آلفا و بتا مشخص کرد. لایه AB در فازهای α و β یکسان است و لایه CD در فاز α با یک صفحه c-glide به AB مرتبط می شود. Si
3N
4 چهاروجهی در Si
3N
4 آلفا و بتا به گونه ای به هم متصل می شوند که تونل ها تشکیل می شوند ، به طور موازی با محور c سلول واحد حرکت داده میشوند. با توجه به صفحه c-glide که AB را به CD مرتبط میکند، ساختار α به جای تونل حاوی حفره است. ساختار مکعبی Si
3N
4 گاما اغلب در ادبیات به عنوان اصلاح c به عنوان اصلاح مکعب نیترید بور (c-BN) تعیین می شود. ساختاری از نوع اسپینل دارد که در آن دو اتم سیلیکون شش اتم نیتروژن را بصورت هشت ضلعی هماهنگ می کنند و یک اتم سیلیسیم چهار اتم نیتروژن را بصورت چهار طرفه هماهنگ می کند. [15]
توالی انباشته شدن طولانی تر باعث می شود که فاز α دارای سختی بیشتری نسبت به فاز β باشد. با این حال ، فاز α در مقایسه با فاز β از نظر شیمیایی ناپایدار است. در دماهای بالا وقتی فاز مایع وجود دارد ، فاز α همیشه به فاز β تبدیل می شود. بنابراین ، سیلیکون نیترید بتا عمده ترین شکل مورد استفاده در سرامیک سیلیکون نیترید است. [16]
علاوه بر چندشکلی های کریستالی نیترید سیلیکون ، ممکن است مواد آمورف شیشه ای به عنوان محصولات پیرولیز پلیمرهای پیش سرامیک تشکیل شود که اغلب حاوی مقادیر مختلفی از کربن باقیمانده هستند (از این رو به طور مناسب تری به عنوان کربنیتریدهای سیلیسیم در نظر گرفته می شوند). به طور خاص ، پلی کربوسیلازان را می توان به راحتی بر روی تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه در اثر تجزیه و تحلیل مواد شیمیایی ، به یک شکل آمورف از ماده بر پایه سیلیکون کربنیترید تبدیل کرد. [17]
استفاده های کاربردی
به طور کلی ، مسئله اصلی در مورد کاربردهای نیترید سیلیکون عملکرد فنی نبوده بلکه هزینه آن بوده است. با کاهش هزینه ها ، تعداد برنامه های تولید در حال شتاب گرفتن است.
صنعت خودرو
یکی از عمده ترین کاربردهای نیترید سیلیسیم پخته شده در صنعت اتومبیل به عنوان ماده ای برای قطعات موتور است. این موارد ، در موتورهای دیزلی ، پلاگین های برقی برای راه اندازی سریعتر شامل می شوند. اتاق های پیش احتراق (اتاق های چرخشی) برای انتشار کمتر ، راه اندازی سریعتر و سر و صدای کمتر. توربوشارژر برای کاهش تاخیر موتور و انتشار آن. در موتورهای احتراق جرقه ای ، از نیترید سیلیسیم برای لنت های بازویی راکر برای سایش کمتر ، توربین های شارژر توربو برای اینرسی کمتر و تأخیر کمتر موتور و در دریچه های کنترل گازهای خروجی برای افزایش شتاب استفاده می شود. به عنوان نمونه هایی از سطح تولید ، تخمین زده می شود که سالانه بیش از 300000 توربوشارژ سیلیکون نیترید متخلخل ساخته می شود. [5] [9]
بلبرینگ

یاتاقانهای نیترید سیلیکون هر دو یاطاقان سرامیکی کامل و یاطاقان ترکیبی سرامیکی با توپی در سرامیک و مسابقات در فولاد هستند. سرامیک های نیترید سیلیکون در مقایسه با سایر سرامیک ها مقاومت در برابر ضربه خوبی دارند. بنابراین ، بلبرینگ های ساخته شده از سرامیک نیترید سیلیکون در بلبرینگ های عملکردی استفاده می شود. یک نمونه نماینده استفاده از یاتاقان های نیترید سیلیکون در موتورهای اصلی شاتل فضایی ناسا است. [18] [19]
از آنجا که یاتاقانهای توپی نیترید سیلیکون از فلز سخت ترند ، این باعث می شود تماس با مسیر یاتاقان کاهش یابد. این منجر به 80٪ اصطکاک کمتر ، 3 تا 10 برابر طول عمر بیشتر ، 80٪ سرعت بالاتر ، 60٪ وزن کمتر ، توانایی کار با گرسنگی روانکاری ، مقاومت در برابر خوردگی بالاتر و درجه حرارت بالاتر عملکرد ، در مقایسه با یاطاقان های فلزی سنتی است. توپهای نیترید سیلیکون 79٪ کمتر از توپهای کاربید تنگستن هستند . بلبرینگ های سیلیکونی نیترید را می توان در بلبرینگ های پیشرفته خودرو ، یاتاقان های صنعتی ، توربین های بادی ، اتومبیلرانی ، دوچرخه ، تخته غلتک و اسکیت بورد یافت . بلبرینگ های نیترید سیلیکون به ویژه در کاربردهایی که استفاده از فلزات در آنها از خوردگی ، میدان های الکتریکی یا مغناطیسی منع شده است بسیار مفید است. به عنوان مثال ، در جریان سنجهای جزر و مدی ، که حمله آب دریا مشکلی ایجاد می کند ، یا در جستجوگران میدان الکتریکی. [9]
Si 3 N 4 اولین بار در سال 1972 به عنوان یك تحمل برتر نشان داده شد اما به دلیل چالش های مرتبط با كاهش هزینه تا سال 1990 به تولید نرسید. از سال 1990 ، با افزایش حجم تولید ، هزینه به میزان قابل توجهی کاهش یافته است. اگرچه سیلیکون نیترید یاتاقان هنوز 2-5 برابر بهترین یاتاقان های فولادی گران ترند ، عملکرد و عمر برتر آنها تصویب سریع را توجیه می کند. حدود 15-20 میلیون سیلیکون نیترید در سال 1996 در ایالات متحده توپ تحمل برای ابزار و ماشین آلات و بسیاری از کاربردهای دیگر تولید شد. رشد سالانه 40٪ تخمین زده می شود ، اما اگر بلبرینگ های سرامیکی برای کاربردهای مصرف کننده مانند اسکیت در خط و درایو دیسک رایانه انتخاب شوند ، می تواند حتی بیشتر باشد.
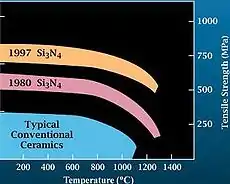
مواد با درجه حرارت بالا

از مدت ها قبل در کاربردهای با درجه حرارت بالا از نیترید سیلیسیم استفاده می شود. به طور خاص ، این ماده به عنوان یکی از معدود مواد سرامیکی یکپارچه شناخته شده است که قادر به زنده ماندن در برابر شوک حرارتی شدید و شیب های حرارتی تولید شده در موتورهای موشکی هیدروژن / اکسیژن است. دانشمندان ناسا برای نشان دادن این قابلیت در یک پیکربندی پیچیده ، از فناوری پیشرفته نمونه سازی سریع برای ساخت یک جزmber محفظه احتراق / نازل (thruster) احتراق قطعه یک اینچ استفاده کردند. راننده با موتور هیدروژن / اکسیژن داغ آزمایش شد و از پنج چرخه از جمله یک چرخه 5 دقیقه ای تا 1320 زنده ماند. C درجه حرارت ماده [20]
در سال 2010 نیترید سیلیکون به عنوان ماده اصلی در رانشگرهای کاوشگر فضایی JAXA Akatsuki استفاده شد . [21]
از نیترید سیلیکون برای "میکرو شاتر" های ساخته شده برای طیف سنج مادون قرمز نزدیک تلسکوپ فضایی جیمز وب استفاده شد . به گفته ناسا: "دمای کار برودتی است بنابراین دستگاه باید بتواند در دمای بسیار سرد کار کند. چالش دیگر تولید کرکره هایی بود که بتوانند: بدون خستگی به طور مکرر باز و بسته شوند. باز کردن به صورت جداگانه و به اندازه کافی باز می شود تا بتواند نیازهای علمی ابزار را برآورده کند. نیترید سیلیکون به دلیل مقاومت بالا و مقاومت در برابر خستگی برای استفاده در میکروشکنها انتخاب شد. " این سیستم میکروشاتر به دستگاه اجازه می دهد تا حداکثر 100 جرم آسمانی را به طور همزمان مشاهده و تجزیه و تحلیل کند. [22]
پزشکی
نیترید سیلیکون کاربردهای ارتوپدی زیادی دارد. [23] [24] این ماده همچنین جایگزینی برای PEEK (پلی اتر اتر كتون) و تیتانیوم است كه برای دستگاههای همجوشی نخاعی استفاده می شود. [25] [26] این سطح هیدروفیلیک ، ریز مخلوط نیترید سیلیکون است که در مقایسه با PEEK و تیتانیوم به مقاومت ، دوام و قابلیت اطمینان مواد کمک می کند. [27]
کارهای اخیر بر روی نیترید سیلیکون نشان داده است که ترکیبات خاصی از این ماده دارای خواص ضد باکتریایی ، [28] خواص ضد قارچی ، [29] و خواص ضد ویروسی است. [30]
ابزار و برش فلز
اولین کاربرد عمده سیلیکون نیترید ابزار ساینده و برش بود . به دلیل سختی ، پایداری حرارتی و مقاومت در برابر سایش ، از نیترید سیلیکون فله ، یکپارچه به عنوان ماده ای برای برش ابزار استفاده می شود . به خصوص برای ماشینکاری با سرعت بالا چدن توصیه می شود. سختی گرم ، مقاومت در برابر شکست و مقاومت در برابر شوک حرارتی به این معنی است که نیترید سیلیکون متخلخل می تواند آلیاژهای پایه چدن ، فولاد سخت و نیکل را با سرعت سطح تا 25 برابر سریعتر از آنهایی که با مواد معمولی مانند کاربید تنگستن بدست می آورند ، برش دهد. [9] استفاده از سیلیکون نیترید ابزار برش تأثیر چشمگیری بر میزان تولید دارد. به عنوان مثال ، تراش صورت چدن خاکستری با درج های نیترید سیلیکون ، سرعت برش را دو برابر افزایش می دهد ، عمر ابزار را از یک قسمت به شش قسمت در هر لبه افزایش می دهد ، و در مقایسه با ابزارهای سنتی کاربید تنگستن ، متوسط هزینه درج ها را 50 درصد کاهش می دهد. [5]
الکترونیک
_process.svg.png.webp)
نیترید سیلیکون اغلب به عنوان عایق و سد شیمیایی در ساخت مدارهای مجتمع ، برای جداسازی الکتریکی ساختارهای مختلف یا به عنوان ماسک اچ در میکروماشین فله استفاده می شود . به عنوان یک لایه انفعال برای ریز تراشه ها ، از دی اکسید سیلیکون برتر است ، زیرا به طور قابل توجهی مانع انتشار در برابر مولکول های آب و یون های سدیم ، دو منبع اصلی خوردگی و بی ثباتی در میکروالکترونیک است. همچنین به عنوان دی الکتریک بین لایه های پلی سیلیکون در خازن ها در تراشه های آنالوگ استفاده می شود.
نیترید سیلیکون رسوب شده توسط LPCVD حاوی حداکثر 8 درصد هیدروژن است. همچنین تنش کششی شدیدی را تجربه می کند که ممکن است باعث ضخامت فیلم های ضخیم تر از 200 شود نانومتر با این حال ، مقاومت و مقاومت دی الکتریک بالاتری نسبت به بسیاری از عایق های معمول در تولید میکرو (10 16 Ω · سانتی متر و 10 به ترتیب MV / cm).
نه تنها نیترید سیلیسیم ، بلکه ترکیبات مختلف سه تایی سیلیکون ، نیتروژن و هیدروژن (SiN x H y ) از لایه های عایق استفاده می شود. آنها با استفاده از واکنشهای زیر پلاسما رسوب می کنند:
این فیلم های SiNH دارای تنش کششی بسیار کمتری هستند ، اما خصوصیات الکتریکی بدتری دارند (مقاومت 10 6 تا 10 15) Ω · سانتی متر ، و قدرت دی الکتریک 1 تا 5 MV / سانتی متر) این فیلمهای سیلیکونی همچنین در شرایط خاص فیزیکی در برابر دمای بالا از نظر حرارتی پایدار هستند. نیترید سیلیکون همچنین به عنوان یکی از لایه های درام عکس در فرایند xerographic استفاده می شود. نیترید سیلیسیم همچنین به عنوان منبع اشتعال برای وسایل گازسوز خانگی استفاده می شود. [31] به دلیل خواص الاستیک خوب ، نیترید سیلیکون ، همراه با اکسید سیلیکون و سیلیکون ، محبوب ترین ماده برای کنسول ها است - عناصر سنجش میکروسکوپ های نیروی اتمی .
تاریخچه
اولین آماده سازی در سال 1857 توسط هنری اتین ساینت-کلر دویل و فردریش وهلر گزارش شد . [32] در روش آنها ، سیلیکون در یک بوته حلقوی شده درون یک بوته بسته بندی شده دیگر با کربن گرم می شد تا از نفوذ اکسیژن به بطری داخلی کاسته شود. آنها محصولی را گزارش دادند که به آن نیترید سیلیکون می گفتند اما بدون تعیین ترکیب شیمیایی آن. پاول شوتزنبرگر ابتدا محصولی را با ترکیب تترانیترید ، سیلیکون نیترید ، در سال 1879 که با حرارت دادن سیلیکون با براسک (خمیری که با مخلوط کردن زغال چوب ، ذغال سنگ یا کک با خاک رس تهیه می شود و سپس برای چیدن بوته ها استفاده می شود) در کوره بلند بدست آمد. در سال 1910 ، لودویگ ویس و تئودور انگلاردت سیلیسیم را تحت نیتروژن خالص گرم کردند تا تولید شود[33] E. Friederich و L. Sittig Si 3 N 4 را در سال 1925 از طریق کاهش کاربوترمال تحت نیتروژن ، یعنی با گرم کردن سیلیس ، کربن و نیتروژن در 1250-1300 درجه سانتیگراد تولید کردند.
نیترید سیلیکون قبل از اینکه در کاربردهای تجاری استفاده شود ، برای دهه ها فقط یک کنجکاوی شیمیایی بود. از سال 1948 تا 1952 ، شرکت Carborundum ، نیاگارا فالز ، نیویورک ، چندین اختراع ثبت شده در زمینه تولید و استفاده از نیترید سیلیکون را درخواست کرد. [5] تا سال 1958 نیترید سیلیکون Haynes ( Union Carbide ) برای تولید لوله های ترموکوپل ، نازل موشک و قایق و بوته های ذوب فلزات در تولید تجاری قرار داشت. کار انگلیس در مورد نیترید سیلیکون ، که در سال 1953 آغاز شد ، با هدف بخشهایی با دمای بالا از توربینهای گازی انجام شد و منجر به تولید نیترید سیلیکون متصل به واکنش و نیترید سیلیکون پرس گرم شد. در سال 1971 ، آژانس پروژه تحقیقات پیشرفته وزارت دفاع ایالات متحده 17 دلار آمریکاقرارداد دو میلیون تومانی با فورد و وستینگهاوس برای دو توربین گازی سرامیکی قرار داد .
حتی اگر خواص نیترید سیلیکون کاملاً شناخته شده بود ، وقوع طبیعی آن فقط در دهه 1990 به عنوان اجزا ریز کشف شد (حدود 2 μm × 0.5 اندازه μm) در شهاب سنگ ها . این ماده معدنی به دلیل پیشگام طیف سنجی جرمی ، آلفرد OC Nier ، نیریت نامگذاری شد. [34] این ماده معدنی ممکن است قبلاً ، فقط به طور انحصاری در شهاب سنگ ها ، توسط زمین شناسان شوروی کشف شده باشد. [35]
منابع
- Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). Boca Raton, FL: CRC Press. p. 4.88. ISBN 1439855110.
- Refractive index database. refractiveindex.info
- ITEM # SI-501, SILICON NITRIDE POWDER MSDS بایگانیشده در ۲۰۱۴-۰۶-۰۶ توسط Wayback Machine. metal-powders-compounds.micronmetals.com
- Carlson, O. N. (1990). "The N-Si (Nitrogen-Silicon) system". Bulletin of Alloy Phase Diagrams. 11 (6): 569–573. doi:10.1007/BF02841719.
- Riley, Frank L. (2004). "Silicon Nitride and Related Materials". Journal of the American Ceramic Society. 83 (2): 245–265. doi:10.1111/j.1151-2916.2000.tb01182.x.
- "Crystec Technology Trading GmbH, Comparison of vertical and horizontal tube furnaces in the semiconductor industry". crystec.com. Retrieved 2009-06-06.
- "Crystec Technology Trading GmbH, deposition of silicon nitride layers". Retrieved 2009-06-06.
- Ghosh Chaudhuri, Mahua; Dey, Rajib; Mitra, Manoj K.; Das, Gopes C.; Mukherjee, Siddhartha (2008). "A novel method for synthesis of α-Si3N4 nanowires by sol-gel route". Science and Technology of Advanced Materials. 9 (1): 5002. Bibcode:2008STAdM...9a5002G. doi:10.1088/1468-6996/9/1/015002. PMC 5099808. PMID 27877939.
- "Silicon Nitride – An Overview". azom.com. 2001-02-06. Retrieved 2009-06-06.
- Nishimura, T.; Xu, X.; Kimoto, K.; Hirosaki, N.; Tanaka, H. (2007). "Fabrication of silicon nitride nanoceramics—Powder preparation and sintering: A review". Science and Technology of Advanced Materials. 8 (7–8): 635. Bibcode:2007STAdM...8..635N. doi:10.1016/j.stam.2007.08.006.
- Peng, p. 38
- "Crystal structures of Si3N4". hardmaterials.de. Retrieved 2009-06-06.
- Jiang, J. Z.; Kragh, F.; Frost, D. J.; Ståhl, K.; Lindelov, H. (2001). "Hardness and thermal stability of cubic silicon nitride". Journal of Physics: Condensed Matter. 13 (22): L515. Bibcode:2001JPCM...13L.515J. doi:10.1088/0953-8984/13/22/111.
- "Properties of gamma-Si3N4". Archived from the original on July 15, 2006. Retrieved 2009-06-06.
- Peng, pp. 1-3
- Zhu, Xinwen; Sakka, Yoshio (2008). "Textured silicon nitride: Processing and anisotropic properties". Science and Technology of Advanced Materials. 9 (3): 3001. Bibcode:2008STAdM...9c3001Z. doi:10.1088/1468-6996/9/3/033001. PMC 5099652. PMID 27877995.
- Wang, Xifan; Schmidt, Franziska; Hanaor, Dorian; Kamm, Paul H.; Li, Shuang; Gurlo, Aleksander (2019). "Additive manufacturing of ceramics from preceramic polymers: A versatile stereolithographic approach assisted by thiol-ene click chemistry". Additive Manufacturing. 27: 80–90. arXiv:1905.02060. Bibcode:2019arXiv190502060W. doi:10.1016/j.addma.2019.02.012.
- "Ceramic Balls Increase Shuttle Engine Bearing Life". NASA. Retrieved 2009-06-06.
- "Space Shuttle Main Engine Enhancements". NASA. Retrieved 2009-06-06.
- Eckel, Andrew J. (1999). "Silicon Nitride Rocket Thrusters Test Fired Successfully". NASA. Archived from the original on April 4, 2009.
- Orbit Control Maneuver Result of the Venus Climate Orbiter 'AKATSUKI'. JAXA (2010-07-06)
- James Webb Space Telescope / Goddard Space Flight Center > Innovations > Microshutters / Nasa (2020-06-25).
- Olofsson, Johanna; Grehk, T. Mikael; Berlind, Torun; Persson, Cecilia; Jacobson, Staffan; Engqvist, Håkan (2012). "Evaluation of silicon nitride as a wear resistant and resorbable alternative for total hip joint replacement". Biomatter. 2 (2): 94–102. doi:10.4161/biom.20710. PMC 3549862. PMID 23507807.
- Mazzocchi, M; Bellosi, A (2008). "On the possibility of silicon nitride as a ceramic for structural orthopaedic implants. Part I: Processing, microstructure, mechanical properties, cytotoxicity". Journal of Materials Science: Materials in Medicine. 19 (8): 2881–7. doi:10.1007/s10856-008-3417-2. PMID 18347952.
- Webster, T.J.; Patel, A.A.; Rahaman, M.N.; Sonny Bal, B. (2012). "Anti-infective and osteointegration properties of silicon nitride, poly(ether ether ketone), and titanium implants". Acta Biomaterialia. 8 (12): 4447–54. doi:10.1016/j.actbio.2012.07.038. PMID 22863905.
- Anderson, MC; Olsen, R (2010). "Bone ingrowth into porous silicon nitride". Journal of Biomedical Materials Research Part A. 92 (4): 1598–605. doi:10.1002/jbm.a.32498. PMID 19437439.
- Arafat, Ahmed; Schroën, Karin; De Smet, Louis C. P. M.; Sudhölter, Ernst J. R.; Zuilhof, Han (2004). "Tailor-Made Functionalization of Silicon Nitride Surfaces". Journal of the American Chemical Society. 126 (28): 8600–1. doi:10.1021/ja0483746. PMID 15250682.
- Pezzotti, Giuseppe; Marin, Elia; Adachi, Tetsuya; Lerussi, Federica; Rondinella, Alfredo; Boschetto, Francesco; Zhu, Wenliang; Kitajima, Takashi; Inada, Kosuke (2018-04-24). "Incorporating Si3 N4 into PEEK to Produce Antibacterial, Osteocondutive, and Radiolucent Spinal Implants". Macromolecular Bioscience. 18 (6): 1800033. doi:10.1002/mabi.201800033. ISSN 1616-5187. PMID 29687593.
- McEntire, B., Bock, R., & Bal, B.S. U.S Application. No. 20200079651. 2020.
- Pezzotti, Giuseppe; Ohgitani, Eriko; Shin-Ya, Masaharu; Adachi, Tetsuya; Marin, Elia; Boschetto, Francesco; Zhu, Wenliang; Mazda, Osam (2020-06-20). "Rapid Inactivation of SARS-CoV-2 by Silicon Nitride, Copper, and Aluminum Nitride". doi:10.1101/2020.06.19.159970. Retrieved 2020-09-21.
- Levinson, L. M. et al. (17 April 2001) "Ignition system for a gas appliance" U.S. Patent ۶٬۲۱۷٬۳۱۲
- "Ueber das Stickstoffsilicium". Annalen der Chemie und Pharmacie. 104 (2): 256. 1857. doi:10.1002/jlac.18571040224.
- Weiss, L.; Engelhardt, T (1910). "Über die Stickstoffverbindungen des Siliciums". Z. Anorg. Allg. Chem. 65 (1): 38–104. doi:10.1002/zaac.19090650107.
- Lee, M. R.; Russell, S. S.; Arden, J. W.; Pillinger, C. T. (1995). "Nierite (Si3N4), a new mineral from ordinary and enstatite chondrites". Meteoritics. 30 (4): 387. Bibcode:1995Metic..30..387L. doi:10.1111/j.1945-5100.1995.tb01142.x.
- "Nierite". Mindat. Retrieved 2009-08-08.