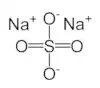
سدیم سولفات
سدیم سولفات نمک سدیم سولفوریک اسید است. در صورتی که بیآب باشد کریستالی سفید با فرمول Na2SO4 تشکیل میدهد که آن را تناردیت نیز مینامند; و هنگام آبپوشی به فرمول Na2SO4·10H2O (دکاهیدرات) تبدیل میشود که به آن نمک گلوبر نیز میگویند. جامد دیگری از آن هپتاهیدرات(Na2SO4·7H2O) است. با تولید سالانه ۶ میلیون تن از پرمصرفترین مواد شیمیایی است.
| سدیم سولفات | |||
|---|---|---|---|
| |||
دیگر نامها تناردیت (معدنی) | |||
| شناساگرها | |||
| شماره ثبت سیایاس | 7757-82-6 7727-73-3 (decahydrate) | ||
| پابکم | 24436 | ||
| کماسپایدر | 22844 | ||
| UNII | 36KCS0R750 | ||
| شمارهٔ آرتیئیسیاس | WE1650000 | ||
| جیمول-تصاویر سه بعدی | Image 1 | ||
SMILES
| |||
| |||
| خصوصیات | |||
| فرمول مولکولی | Na2SO4 | ||
| جرم مولی | 142.04 g/mol (anhydrous) 322.20 g/mol (decahydrate) | ||
| شکل ظاهری | white crystalline solid hygroscopic | ||
| چگالی | 2.664 g/cm3 (anhydrous) 1.464 g/cm3 (decahydrate) | ||
| دمای ذوب | 884 °C (anhydrous) 32.4 °C (decahydrate) | ||
| دمای جوش | 1429 °C (anhydrous) | ||
| انحلالپذیری در آب | 47.6 g/L (0 °C) 427 g/L (100 °C) | ||
| انحلالپذیری | نامحلول در اتانول | ||
| ضریب شکست (nD) | 1.468 (anhydrous) 1.394 (decahydrate) | ||
| ساختار | |||
| ساختار بلوری | اورتورومبیک یا شانزدهتایی (anhydrous) مونوکلینیک (decahydrate) | ||
| خطرات | |||
| MSDS | ICSC 0952 | ||
| شاخص ئییو | فهرست نشده | ||
| خطرات اصلی | مضر | ||
| لوزی آتش | |||
| نقطه اشتعال | |||
| ترکیبات مرتبط | |||
| دیگر آنیونها | سدیم سلنات سدیم تلورات | ||
| دیگر کاتیونها | لیتیم سولفات پتاسیم سولفات روبیدیم سولفات سزیم سولفات | ||
| ترکیبات مرتبط | سدیم بیسولفات سدیم سولفیت سدیم پرسولفات | ||
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |||
| | |||
| Infobox references | |||
|
| |||
این ماده در تولید مواد شوینده و تهیه خمیر کاغذ کاربرد دارد. معمولاً در طبیعت به شکل دکاهیدارت یافت میشود. سولفات سدیم | Sodium Sulfate
نام علمی
سولفات سدیم: نمک سدیم سولفوریک اسید
فرمول شیمیایی : Na2SO4
سدیم سولفات تناردیت با فرمول Na2SO4
سدیم سولفات دکاهیدرات با فرمول Na2SO4·۱۰H2O
سدیم سولفات هپتاهیدرات با فرمول (Na2SO4·۷H2O) نمک گلوبر
سولفات سدیم در طبیعت
سدیم سولفات یکی از عمومیترین مواد بسیاری از آبهای معدنی همانند آب دریا میباشد، همچنین سولفات در ریزشهای جوی وجود داشته و یکی از اصلیترین محلولهای موجود در برف و باران میباشد. بسیاری از دریاچههای شور در سرتاسر دنیا مقادیر مختلفی سولفات سدیم دارند. این ماده از نظر شیمیایی بسیار پایدار است.
سولفات سدیم به عنوان یک ماده معدنی در طبیعت یافت میشود و یا از طریق برخی از فرایندهای صنعتی به عنوان یک محصول جانبی تولید میشود. سولفات سدیم در رده مواد شیمیایی غیرسمی در شرایط عادی قرار گرفته و کاربردهای صنعتی فراوانی دارد . این ماده با گرید و خلوص مختلف در صنایع مختلفی همچون شیشه سازی، دارو سازی، بافندگی ، مواد شوینده و …. کاربرد فراوان دارد.
کاربرد در صنعت
خوراک دام
صنایع داروسازی
صنایع شیشه سازی
صنایع پودر شوینده و پاککننده
صنایع بافندگی و صنعت رنگرزی
صنایع نظامی ,عکاسی, سولفور سدیم
صنایع کاغذ ( کاغذ کرافت ) و غیره ….
کاربرد در صابون و مواد شوینده
بخش عمدهای از مصرف سولفات سدیم در مواد شوینده در طول سالیان اخیر به عنوان یک ماده پرکننده بودهاست. البته کاربرد سولفات سدیم به عنوان پرکننده در شویندههای پودری رو به کاهش است که این موضوع ناشی از رویکردی است که در زمینه استفاده از شویندههای مایع غلیظ به جای استفاده از فرمولهای پودری که حجیم تر هم هستند پدید آمدهاست.
کاربرد در صنایع رنگرزی و نساجی
سالانه صدها هزار تن سولفات سدیم در جهان در صنایع نساجی برای رنگرزی پارچهها استفاده میشود. این ماده موجب نفوذ یکنواخت و هم سطح رنگ درون بافتهای پارچه میشود و بر خلاف کلرید سدیم موجب زنگ زدگی لولههای فولادی نمیشود. سولفات سدیم در رنگرزی به عنوان تعدیلکننده بارهای روی سطح منسوج و پارچه، در چاپ کالاهای نساجی کاربرد دارد.
کاربرد در صنایع کاغذ و چوب
سولفات سدیم کاربرد فراوانی در صنعت کاغذ و چوب (پالپ چوب) در فرایند کرافت (فرایند سولفات) به منظور تولید پالپ چوب دارد و بهطور گسترده در ساخت کاغذ و برخی از مواد ساختمانی استفاده میشود.
کاربرد در صنایع شیشهسازی
سولفات سدیم صنایع شیشهسازی و شیشهآلات نیز کاربرد دارد. سولفات سدیم مانع از به وجود آمدن سفیدی توسط شیشهٔ مذاب در طی پالایش میشود. سولفات سدیم به عنوان عامل استخراجی در شیشهٔ ذوب شده عمل مینماید و موجب حذف حبابهای کوچک هوا در فرایندهای دمیدن و قالبسازی شیشه میشود.
ایمنی
اگرچه سدیم سولفات به عنوان یک مادهٔ غیرسمی شناخته میشود,[1] اما باید با دقت استفاده شود. غبار آن میتواند به آسم موقت یا صدمات چشمی منجر شود اما به راحتی با محافظ چشم یا ماسک میتوان از آن جلوگیری کرد. حمل و نقل آن محدود نشدهاست و در فهرست ایمنی و حفاظتی قرار ندارد.[2]
منابع
- "Sodium sulfate (WHO Food Additives Series 44)". سازمان بهداشت جهانی. 2000. Retrieved 2007-06-06.
- "MSDS Sodium Sulfate Anhydrous". James T Baker. 2006. Archived from the original on 28 May 2007. Retrieved 2007-04-21.