کروم
کروم (به انگلیسی: Chromium) یک عنصر شیمیایی با نماد Cr و عدد اتمی ۲۴ است. این عنصر اولین عنصر در گروه ۶ است. کروم یک فلز واسطه است که رنگی خاکستری، و سطحی براق داشته، و [[سختی|سخت] و نسبت به سایر فلزات جامد شکننده تر است..[3] کروم افزودنی اصلی در تولید فولاد زنگ نزن است که باعث خاصیت ضد خوردگی آن میشود.همچنین از کروم در ساخت ظروف استیل استفاده می شود. همچنین کروم به عنوان فلزی که دارای خاصیت جلاپذیری بالا بوده و در مقابل کدر شدن نیز مقاومت بسیار خوبی دارد از اهمیت فراوانی برخوردار است. کروم صیقل کاری شده تقریباً ۷۰٪ از طیف مرئی و تقریباً ۹۰٪ از نور مادون قرمز را منعکس میکند.[4] نام این عنصر از کلمه یونانی χρῶμα، chrōma به معنی رنگ گرفته شدهاست،[5] زیرا بسیاری از ترکیبات کروم به شدت رنگی هستند.
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| کروم | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ظاهر | نقرهy metallic | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| جرم اتمی استاندارد (Ar، استاندارد) | ۵۱٫۹۹۶۱(۶)[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| کروم در جدول تناوبی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| عدد اتمی (Z) | 24 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| گروه | گروه ۱۲ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دوره | دوره 4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| بلوک | بلوک-d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دسته | Transition metal | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| آرایش الکترونی | [Ar] 3d5 4s1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2, 8, 13, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ویژگیهای فیزیکی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| فاز در STP | جامد | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطه ذوب | 2180 K (1907 °C, 3465 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطه جوش | 2944 K (2671 °C, 4840 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| چگالی (near r.t.) | 7.19 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| در حالت مایع (at m.p.) | 6.3 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| حرارت همجوشی | 21.0 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| آنتالپی تبخیر | 339.5 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ظرفیت حرارتی مولی | 23.35 J/(mol·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
فشار بخار
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ویژگیهای اتمی | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| عدد اکسایش | −4, −2, −1, 0, +1, +2, +3, +4, +5, +6 (depending on the oxidation state, an acidic, basic, or amphoteric اکسید) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الکترونگاتیوی | مقیاس پائولینگ: 1.66 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| انرژی یونش |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شعاع اتمی | empirical: 128 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شعاع کووالانسی | pm 139±5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Color lines in a spectral range | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| دیگر ویژگی ها | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ساختار بلوری | (bcc) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سرعت صوت thin rod | 5940 m/s (at 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| انبساط حرارتی | 4.9 µm/(m·K) (at 25 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رسانندگی گرمایی | 93.9 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رسانش الکتریکی | 125 n Ω·m (at 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رسانش مغناطیسی | AFM (rather: SDW[2]) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| مدول یانگ | 279 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| مدول برشی | 115 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| مدول حجمی | 160 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نسبت پواسون | 0.21 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سختی موس | 8.5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سختی ویکرز | 1060 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سختی برینل | 1120 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شماره ثبت سیایاس | 7440-47-3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ایزوتوپهای کروم | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
آلیاژ فِروکروم به صورت تجاری از طریق واکنشهای سیلیکوترمی یا آلومینوترمی کرومیت تولید میشود و فلز کروم با فرایندهای پخت (roasting) و سنگ شویی و سپس کاهش کربن و آلومینیوم تولید میشود. فلز کروم از نظر مقاومت در برابر خوردگی و سختی بالا از ارزش بالایی برخوردار است. یک پیشرفت عمده در تولید فولاد کشف این بود که میتوان با افزودن کروم فلزی به فولاد آن را شدیداً در برابر خوردگی و تغییر رنگ مقاوم کرد و فولاد زنگ نزن تولید کرد. تولید فولاد زنگ نزن و آبکاری کروم در کنار هم حدود ۸۵٪ از مصرف تجاری کروم را تشکیل میدهند.
بزرگترین تولیدکنندگان سنگ کروم در سال ۲۰۱۹ آفریقای جنوبی (۳۹٪)، ترکیه (۲۳٪)، قزاقستان (۱۵٪) و هند (۹٪) بودهاند، و ۱۴٪ باقی مانده مربوط به سایر کشورها است.[6] ارزش بازار جهانی کروم در سال ۲۰۱۶ برابر ۱۳٫۰۷ میلیارد دلار بوده و پیشبینی میشود این مقدار در سال ۲۰۲۵ به ۱۶٫۵۵ میلیارد دلار برسد.[7]
تاریخچه
یوهان گوتلوب لمن در سال ۱۷۶۱ در کوههای اورال ماده معدنی نارنجی-قرمز رنگی پیدا کرد که نام آن را سرب قرمز سیبریایی نهاد. گرچه او به اشتباه آن را ترکیب سرب با آهن و سلنیوم انگاشت، آن ماده معدنی در حقیقت کرومات سرب (PbCrO4) بود.
پیتر سیمون پالاس در سال ۱۷۷۰ این ماده معدنی سربی قرمزرنگ (سرب قرمز سیبریایی) را در همان مکانی که لمن قبلاً دیده بود، مشاهده کرد که خصوصیات مفید زیادی داشت. از جمله این خصوصیات کاربرد آن به عنوان رنگدانه در تولید رنگ بود که استفاده از این ویژگی به سرعت توسعه یافت. رنگ زرد درخشانی که از کروکوئیت ساخته شد به یک رنگ بسیار رایج تبدیل گشت.
سال ۱۷۹۷ نیکلاس لوئی واکلین نمونههایی از سنگ معدن کروکوئیت را پیدا کرد. او با مخلوط کردن کروکوئیت و اسید هیدروکلریک موفق به تهیه اکسید کروم (CrO3) گشت. سال ۱۷۹۸ واکلین متوجه شد که با حرارت دادن این اکسید در کورههای ذغالی میتوان کروم فلزی به دست آورد. او موفق به شناسایی مقدار کمی کروم در سنگهای قیمتی از جمله یاقوت و زمرد شد.
در طول دهه اول قرن نوزدهم از کروم بیشتر به عنوان سازهای در رنگها استفاده میشد، اما امروزه عمده کاربرد آن (۸۵٪) در آلیاژهای فلزی است و مابقی موارد استفاده آن در صنایع شیمیایی، مواد نسوز و صنایع پایه است.
کاربردها
موارد استفاده کروم:
- در متالورژی برای مقاوم کردن در مقابل پوسیدگی و در براقی نهائی:
- بهعنوان یک جزء در آلیاژها، مثلاً در فولاد ضدزنگ،
- در آب کاری با کروم،
- در آلومینیوم آنادایز،
- به عنوان یک کاتالیزور.
- از کرومیت برای ساخت قالبهای پخت آجر استفاده میشود.
- نمکهای کروم باعث سبز شدن رنگ شیشه میشوند.
- کروماتها و اکسیدها در رنگ مو و رنگهای معمولی به کار میروند.
- دی کرومات پتاسیم یک معرف شیمیایی است که درتمیز کردن ظروف شیشهای آزمایشگاهی و به عنوان یک عامل تیترات مورد استفاده قرار میگیرد. این عنصر همچنین به صورت دندانه (مثلاً، عامل ثابت نگه دارنده) در رنگرزی بکار میرود.
- دیاکسید کروم(CrO2) در تولید نوارهای مغناطیسی مصرف میشود این نوارها نسبت به نوارهای اکسید آهن دارای مقاومت در برابر میدانهای مغناطیسی بیشتری بوده، لذا کارایی بهتری دارند.
- جهت دوپ کردن در پوشش کربن شبه الماس (DLC)
نقش بیولوژیکی
کروم سه ظرفیتی فلزی است که مقدار کم آن بسیار ضروری است و برای سوخت و ساز کامل قند در بدن انسان مورد نیاز است. کمبودهای کروم میتواند بر توانایی انسولین در ثابت نگهداشتن میزان قند خون تأثیر بگذارد. برخلاف سایر فلزاتی که مقدار کم آنها ضروری است، برای کروم عملکرد بیولوژیکی در متالوپروتئین دیده نشدهاست.
خاصیت ضدزنگ کردن
این فلز کروم میتواند بسیاری از فلزات دیگر را ضدزنگ کرده و از آنها در برابر خوردگی و زنگ زدن محافظت کند. از همین رو یکی از آلیاژهای اصلی فولاد ضدزنگ یا استینلس استیل را کروم تشکیل میشود.
البته باید مد نظر قرارداد که زیر ۴ درصد کروم، خاصیت ضدزنگ ایجاد نمیکند.
حضور کروم زیر چهار درصد در کنار کربن به استحکام قطعه میافزاید.
پیدایش
کروم به شکل سنگ معدن کرومیت Fe, Mg)Cr2O۴) استخراج میشود و با غلظت ۲۱ ذره در میلیون بیستویکمین عنصر از نظر فراوانی در پوسته زمین است. این عنصر را به صورت تجاری با حرارت دادن این سنگ معدن در حضور آلومینیوم یا سیلیسیوم تهیه میشود. نزدیک به نیمی از سنگ معدن کرومیت جهان در آفریقای جنوبی تولید میشود و قزاقستان، هند، زیمبابوه، ایران، فنلاند، برزیل، روسیه و ترکیه نیز از تولیدکنندگان عمده آن هستند. مقدار کرومیت استخراج نشده بسیار زیاد است، اما از نظر جغرافیایی در قزاقستان و آفریقای جنوبی متمرکز هستند. در سال ۲۰۰۰ حدود ۴٫۴ میلیون تن سنگ معدن کرومیت قابل فروش تولید شد که ۳٫۳ میلیون تن آهن- کروم به ارزش تقریبی ۲٫۵ میلیارد دلار آمریکا از آن به دست آمد.
اگرچه وجود کروم خالص بسیار نادر است، مقادیری کروم خالص کشف شدهاست. معدن اوداچنایا در روسیه نمونههایی از کروم خالص تولید میکند. این معدن یک استوانه کیمبرلیت غنی از الماس است که در آن هم کروم خالص و هم الماس تولید میشود.
تولید

در سال ۲۰۱۳ تقریباً ۲۸٫۸ میلیون تن سنگ معدن کرومیت قابل فروش تولید شده و به ۷٫۵ تن فِروکروم تبدیل شد.[8] طبق تحقیقات سازمان زمینشناسی آمریکا، «فروکروم اصلیترین کاربرد نهایی سنگ معدنی کرومیت بوده، و تولید فولاد زنگ نزن اصلیترین کاربرد فروکروم است.»[9]

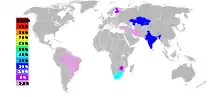
بزرگترین تولیدکنندگان سنگ کروم در سال ۲۰۱۹ به ترتیب آفریقای جنوبی (۳۹٪)، ترکیه (۲۳٪)، قزاقستان (۱۵٪) و هند (۹٪) بودهاند، و ۱۴٪ باقی مانده مربوط به سایر کشورها است.[6]
دو محصول اصلی تصفیه سنگ کروم، فروکروم و کروم فلزی هستند. فرایند تولید این دو محصول تفاوت زیادی با هم دارد. برای تولید فروکروم، سنگ معدن کرومیت (FeCr2O4) در مقیاس بزرگ در کوره قوس الکتریکی یا در کارخانههای ذوب کوچکتر، با آلومینیوم یا سیلیسیم در یک واکنش آلومینوترمی کاهش مییابد.[10]
برای تولید کروم خالص، آهن باید در یک فرایند دو مرحله ای پخت و سنگ شویی از کروم جدا شود. سنگ معدن کرومیت با مخلوطی از کربنات کلسیم و کربنات سدیم در حضور هوا گرم میشود. کروم اکسید شده و به شکل شش ظرفیتی تبدیل میشود، در حالی که آهن به شکل پایدار Fe2O3 تبدیل میشود. سپس سنگ شویی در دمای بالاتر باعث حل شدن کروماتها شده و اکسید آهن نامحلول را باقی میگذارد. کرومات توسط اسید سولفوریک به دی کرومات تبدیل میشود.[11] دی کرومات با کاهش با کربن به اکسید کروم (III) تبدیل میشود و سپس در واکنش آلومینوترمی به کروم کاهش مییابد.[12]
ترکیبات
دی کرومات پتاسیم عامل اکسیدکننده بسیار قوی است و این ترکیب برای تمیز کردن ظروف آزمایشگاهی، ارجح تر از سایر ترکیبات آلی است. اکسید کرومیک همان اکسید کروم سبز است (Cr2O۳)که در نقاشی لعابی و رنگ کردن شیشه مورد استفاده قرار میگیرد. زردینه کروم رنگدانه زرد درخشانی است (PbCrO4) که مورد استفاده نقاشان قرار میگیرد. اسید کرومیک دارای ساختار فرضی H2CrO۴ است. نه اسید کرومیک و نه اسید دی کرومیک در طبیعت یافت نمیشوند اما آنیونهای آنها در ترکیبات متنوعی یافت میشود. تریاکسید کروم CrO۳، اسید بدون آب اسید کرومیک - به صورت تجاری، بهعنوان اسید کرومیک بفروش میرسد.
ایزوتوپها
کروم بهطور طبیعی متشکل از ۳ ایزوتوپ پایدار Cr-53 ,Cr-54 ,Cr-۵۲ است که فراوانترین آنها Cr-۵۲ (با فراوانی طبیعی ۷۸۹/۸۳٪) است. ۱۹ رادیو ایزوتوپ که پایدارترین آنها Cr-۵۰ با نیمه عمر (بیش از) ۱٫۸E۱۷سال وCr-۵۱ با نیمه عمر۷۰۲۵/۲۷ روز است برای این عنصر شناخته شدهاست. مابقی ایزوتوپهای رادیواکتیو آن از نیمه عمری کمتراز ۲۴ ساعت برخوردارند که نیمه عمر اکثر آنها کمتر از ۱ دقیقه است. این عنصر همچنین دارای ۲ حالت برانگیخته است. کروم ۵۳ محصول فروپاشی پرتوزاد Mn-۵۳ است. محتویات ایزوتوپی کروم معمولاً با محتویات ایزوتوپی منگنز ترکیب میشود و در زمینشناسی ایزوتوپی کاربرد دارد. نسبتهای ایزوتوپ Mn-Cr شواهدی را که از Al-۲۶ وPd-۱۰۷ دربارهٔ تاریخ ابتدایی به دست آمده تقویت میکند. اختلاف در نسبتهای Cr-53/Cr-۵۲ و Mn-Cr در چندین شهاب سنگ بیانگر یک نسبت Mn-53/Mn-۵۵ است که نشان میدهد ردهبندی ایزوتوپ Mn-Cr باید از فروپاشی ثابت Mn-۵۳ در پیکره سیارههای مجزا ناشی شده باشد؛ بنابراین Cr-۵۳ دلایلی بیشتر را دربارهٔ فرایندهای نوکلئوسنتزی بلافاصله قبل از یکپارچگی منظومه شمسی در اختیار میگذارد.
ایزوتوپهای کروم از نظر وزن اتمی، در بازه ۴۳amu (کروم ۴۳) تا ۶۷amu(کروم ۶۷) قرار دارند. حالت فروپاشی اتمی بلافاصله قبل از فراوانترین ایزوتوپ پایدار (کروم ۵۲)، جذب الکترون است و حالت بلافاصله بعد از آن کاهش بتا است.
هشدارها
فلز کروم و ترکیبات کروم (III) معمولاً" برای سلامتی خطرناک نیستند، اما ترکیبات کروم VI در صورت بلع سمی هستند. مقدار تقریباً" نصف قاشق چای خوری ترکیبات کروم سمی (VI) کشنده بوده و سرطانزا بودن مقادیر غیرکشنده کروم VI به اثبات رسیدهاست. بیشتر ترکیبات کروم VI برای چشم، پوست و همچنین بافتهای مخاطی مضر هستند. تماس دائمی با این ترکیبات میتواند موجب آسیبهای دائمی چشم گردد، مگر مواردی که درمان کامل صورت پذیرد.
در سال ۱۹۵۸ سازمان بهداشت جهانی حداکثر میزان مصرف مجاز کروم VI از جنبه سلامتی را ۰۵/۰ میلیگرم در هر لیتر آب آشامیدنی پیشنهاد کرد. این پیشنهاد بارها بررسی شد و در این فاصله مقدار اعلام شده تغییر نکرد
منابع
- Meija, J.; et al. (2016). "Atomic weights of the elements 2013 (IUPAC Technical Report)". شیمی محض و کاربردی(نشریه). 88 (3): 265–91. doi:10.1515/pac-2015-0305.
- Fawcett, Eric (1988). "Spin-density-wave antiferromagnetism in chromium". Reviews of Modern Physics. 60: 209. doi:10.1103/RevModPhys.60.209.
- Brandes, EA; Greenaway, HT; Stone, HEN (1956). "Ductility in Chromium". Nature. 178 (4533): 587. Bibcode:1956Natur.178..587B. doi:10.1038/178587a0. S2CID 4221048.
- Coblentz, WW; Stair, R. "Reflecting power of beryllium, chromium, and several other metals" (PDF). National Institute of Standards and Technology. NIST Publications. Retrieved 11 October 2018.
- χρῶμα, Henry George Liddell, Robert Scott, A Greek-English Lexicon, on Perseus
- "Chromium mine production worldwide by country 2019". Statista. Retrieved 2020-12-21.
- "Chromium Market Size Worth $16.55 Billion By 2025 | CAGR: 2.7%". www.grandviewresearch.com. Retrieved 2020-12-21.
- Papp, John F. "Mineral Yearbook 2015: Chromium" (PDF). United States Geological Survey. Retrieved 3 June 2015.
- Papp, John F. "Mineral Yearbook 2015: Chromium" (PDF). United States Geological Survey. Retrieved 3 June 2015.
- Papp, John F.; Lipin, Bruce R. (2006). "Chromite". Industrial Minerals & Rocks: Commodities, Markets, and Uses (7th ed.). SME. ISBN 978-0-87335-233-8.
- Papp, John F.; Lipin, Bruce R. (2006). "Chromite". Industrial Minerals & Rocks: Commodities, Markets, and Uses (7th ed.). SME. ISBN 978-0-87335-233-8.
- Papp, John F.; Lipin, Bruce R. (2006). "Chromite". Industrial Minerals & Rocks: Commodities, Markets, and Uses (7th ed.). SME. ISBN 978-0-87335-233-8.
- آزمایشگاه ملی لوسآلاموس - کرومیوم (به انگلیسی).
پیوند به بیرون
- WebElements.com - Chromium
- EnvironmentalChemistry.com - Chromium
- International Chromium Development Association بایگانیشده در ۲۹ نوامبر ۲۰۰۳ توسط Wayback Machine
- It's Elemental - The Element Chromium
- Native Chromium
- The Merck Manual - Mineral Deficiency and Toxicity